・合成高分子化合物
【目次】
(1) 高分子化合物の分類
普通の化合物の分子量は、500以下であることがほとんどです。それに対し、分子量が1万を超えるような巨大分子を「高分子(polymer)」といい、その化合物を「高分子化合物(macromolecule)」といいます。高分子化合物は、炭素Cを主な骨格とした有機物である「有機高分子化合物(organic polymer)」と、ケイ素Siや酸素Oなどを主な骨格とした無機物である「無機高分子化合物(inorganic polymer)」に分類されます。高分子化合物といえば、一般的に有機高分子化合物の方を指すことが多いです。また、高分子化合物のうち、デンプンやケイ酸塩などのように天然に存在するものを「天然高分子化合物(natural polymer)」といい、ポリエチレンやナイロンなどのように人工的に合成したものを「合成高分子化合物(synthetic polymer)」といいます。
表.1 高分子化合物の分類と例
|
分類 |
天然高分子化合物 |
合成高分子化合物 |
|
有機高分子化合物 |
デンプン、セルロース、タンパク質、天然ゴム |
ポリエチレン、ナイロン、ポリエステル、フェノール樹脂、尿素樹脂、合成ゴム |
|
無機高分子化合物 |
水晶、雲母、長石、石綿(アスベスト) |
ガラス、シリカゲル、合成ルビー、シリコーン樹脂 |
多くの高分子化合物は、小さな構成単位が繰り返し結合した形をしています。この構成単位となる小さな分子を「単量体(monomer)」といい、この単量体が次々に結合する反応を「重合(polymerization)」、重合により生じる高分子化合物を「重合体(polymer)」といいます。重合体は、その作り方によって、2つの主なグループに分類できます。
(i) 付加重合
「付加重合体(addition polymer)」は、単量体が他の単量体に繰り返し付加することで、でき上がるものです。この単量体は、一般的にアルケンCnH2nであって、不飽和結合を持つ単量体が次々に付加反応し、付加反応の繰り返しで進行する重合を、「付加重合(addition polymerization)」といいます。また、2種類以上の異なる単量体を混合して行う重合を、「共重合(copolymerization)」といいます。
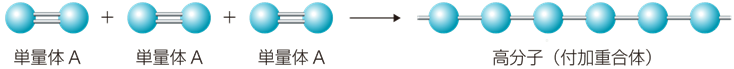
図.1 付加重合は、付加反応の繰り返しで進行する重合である
この重合反応には、触媒または開始剤が必要で、これが炭素-炭素二重結合に付加して、活性中間体を生じます。そして、この中間体が2番目の単量体の二重結合に付加して、新たな中間体を生じます。この反応工程は、最終的にある形で反応が停止するまで連続して進行し、重合体鎖が形成されます。したがって、重付加重合体は、単量体単位に含まれる原子を、すべて重合体中に保持することになります。この重付加重合体の最も良い例は、「ポリエチレン」です。

図.2 ポリエチレンの合成反応
(ii) 縮合重合
「縮合重合体(condensation polymer)」は、単量体が他の単量体と繰り返し縮合することで、でき上がるものです。縮合反応の繰り返しで進行する重合を、「縮合重合(condensation polymerization)」といいます。縮合重合は、一般的に2つの異なる官能基間の反応で形成されるものであり、そこでは水H2Oのように小さな分子が失われます。したがって、重縮合重合体は、単量体単位に存在した原子を、必ずしも含まないことになり、その部分は、小さな脱離分子となって失われます。
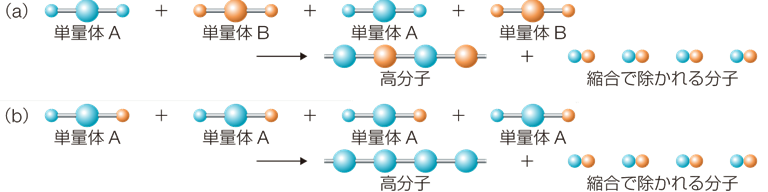
図.3 縮合重合は、縮合反応の繰り返しで進行する重合である
ここで使用される単量体単位は、縮合を行う官能基が一般的に複数存在し、重合体分子中では、単量体単位が交互に存在することになります。重縮合重合体の好例は、ポリアミドの「6,6-ナイロン」です。これは、ヘキサメチレンジアミン(1,6-ジアミノヘキサン)とアジピン酸(ヘキサン二酸)を縮合重合させて製造されています。
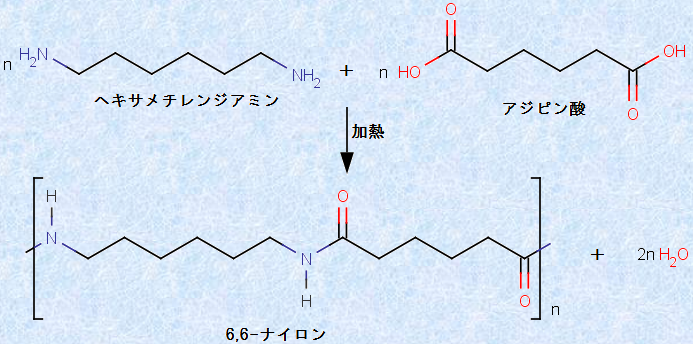
図.4 6,6-ナイロンの合成反応
(2) 合成繊維
「合成繊維(synthtic fiber)」は、単量体を重合させて合成した鎖状の高分子を、紡糸することによって得られます。単量体の結合様式によって分類され、代表的なものとして、「ポリアミド系合成繊維」・「ポリエステル系合成繊維」・「ポリアクリロニトリル系合成繊維」・「ポリビニル系合成繊維」などがあります。
(i) ナイロン
アミド結合(-NHCO-)により重合した合成繊維を、「ポリアミド系合成繊維」といい、一般的に「ナイロン」と呼ばれています。主なナイロンには、「6,6-ナイロン(ナイロン66)」や「6-ナイロン(ナイロン6)」などがあります。ナイロンは、当時非常に高価であった絹糸の代用品として、世界で初めて開発された合成繊維でした。世界に冠たる生糸と絹の生産国であった日本は、絹に代わる繊維としてのナイロンの登場に、大きな衝撃を受けました。
「6,6-ナイロン」は、1935年にアメリカの化学メーカーであるデュポン社の研究員ウォーレス・カロザースのグループによって、初めて作られた合成繊維です。それから3年後の1938年にナイロンの誕生が世に発表され、1940年に工業化に成功しました。当時、化学の世界では「高分子は実在するのか」という論争が展開されており、カロザースは、高分子説の真偽を実験的に検証しようと考えていたのです。カロザースのアプローチは、低分子を既知の有機化学反応を使って、逐一繋ぎ合わせることによって、高分子を人工的に合成しようと試みるものでした。カロザースが合成した6,6-ナイロンは、炭素数が6個のヘキサメチレンジアミンと、同じく炭素数が6個のアジピン酸を縮合重合して作られます。名称にある最初の6はジアミン成分の炭素数を、後ろの6は2価カルボン酸の炭素数を意味します。
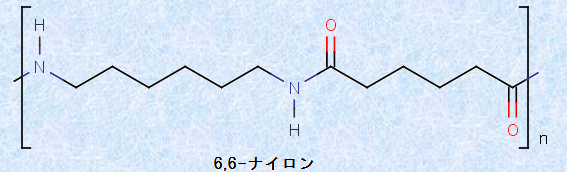
図.5 6,6-ナイロンの構造式
6,6-ナイロンは、化学構造が絹によく似ており、絹のような光沢や感触があります。さらに、摩耗や薬品に強く、防虫性にも優れています。短所としては、吸湿性に乏しく、熱に弱いことがあげられます。「石炭と水と空気から作られ、鋼鉄よりも強く、クモの糸より細い夢の繊維」というデュポン社のキャッチフレーズが示すように、天然繊維と比べて丈夫で軽く、弾力があったので、今日においても、衣料用繊維として広く使用されています。最初から製品化を目指した研究ではなく、純粋に学術的な研究からこうした成果が生まれたことは、大変に興味深いことです。
6,6-ナイロンが開発されるまでは、女性用のストッキングは、絹でできていました。しかし、絹製のストッキングは繊細で高価、その上に品薄でした。1940年5月、初めて売り出されたナイロン製のストッキングは、大変に好評で、500万足のストッキングが、たった4日で売り切れたといわれています。ナイロン製のストッキングが発売されてからは、たった数年で、6,400万足ほどのストッキングが売れました。これは、当時のアメリカにいた大人の女性の数より多いというのだから驚きです。ナイロン製のストッキングは、簡単に買える安さで、しかも格好も良く、女性たちを魅了しました。カロザースの発明が契機となり、世界中で人工的に高分子化合物を作ろうとする動きが加速したのです。
ちなみに、「ナイロン(nylon)」の名前は、ストッキングが「no run(伝線しない)」に由来します。しかし、実際にはナイロンは伝線することがあるので、oとuを入れ替えて「nuron」としました。その後、語呂を調整して「nulon」から「nilon」となり、最終的に「nylon」となったのです。それまでの日本産の絹製の靴下に代わる丈夫なストッキングは、たちまち人気商品となりました。現在でも、アメリカではストッキングのことを、ナイロンと呼んでいるそうです。

図.6 ナイロン製のストッキングを眺める女性
ナイロンは、デュポン社にその事業規模を倍にするほどの収益をもたらしましたが、カロザースの最期は随分と悲惨なものでした。もともとハーバード大学の有機化学の講師だったカロザースは、1928年に32歳の若さでデュポン社の有機化学研究所の基礎研究プログラムの部長として迎えられました。デュポン社で基礎研究に打ち込み、ナイロンを発見したグループのプロジェクトリーダーでしたが、ナイロンの生産体制からは外されました。その後、カロザースは、ナイロンで成功を収めたにもかかわらず、「自分は何も達成できておらず、才能が枯渇した」と考えるようになります。そして、アルコール依存症と重度の鬱病の果てに、1937年4月28日、フィラデルフィアのペンシルバニア大学に近いホテルの一室で、青酸カリKCNを混ぜたレモンジュースを飲んで、自殺してしまいました。化学者であるカロザースは、酸性溶液が、青酸の毒性を強めることを知っていたのです。カロザースは2日前に41歳の誕生日を迎えたばかりで、彼の娘は7か月後の11月27日に誕生しました。
カロザースの発明したナイロンは、綿や絹などの天然繊維から合成繊維への転換をもたらし、世界を変える偉大な発明でした。しかしながら、死亡した当時は、ナイロンはデュポン社の企業秘密であったため、功績の大きさにもかかわらず、カロザースは無名のままこの世を去りました。2000年11月、没後60年以上が経過して、カロザースはようやく、アメリカ科学復興協会から表彰を受けることになります。カロザースは、生涯中に高分子に関する52の論文、69の米国特許を取り、高分子化学工業発展の大きな基盤を作りました。存命ならば、ノーベル化学賞は確実だったとの評価もあります。

図.7 カロザースは偉大な発明をしたが、アルコール依存症と鬱病の果てに自ら命を絶った
6,6-ナイロンの登場により、一番困ったのは日本でした。主要な輸出品である絹の価格が大暴落したからです。1939年にニューヨークの万国博覧会で、6,6-ナイロンは「人工絹」として脚光を浴び、その後の絹産業に大きな影響を与えたのです。当時、日本の生糸の輸出先の大部分はアメリカでした。もしナイロンによって日本の生糸がアメリカから締め出された場合、日本の何十万という繊維業者はもちろん、蚕を飼って暮らしてきた何百万の農家にとって大事件です。そのため、対抗策として日本発の新しい合成繊維の開発が急がれました。
その結果、1941年に日本の東洋レーヨンの星野孝平らによって、「6-ナイロン」が開発されました。ε -カプロラクタムに少量の水などを加えて約260℃で加熱し、減圧下で水分を除去しながら反応させると、7員環が開いてアミノ基(-NH2)が生成します。そして、これが2番目のε -カプロラクタム分子のカルボニル基(-CO-)と反応します。すると、そこからまた新たにアミノ基(-NH2)が生成し、次の分子と反応します。このようにして、次々と環内のアミド結合(-NHCO-)が切れて重合が進み、鎖状の6-ナイロンが生じるのです。このような環式化合物の開環を伴う重合を、「開環重合(ring-opening polymerization)」といいます。
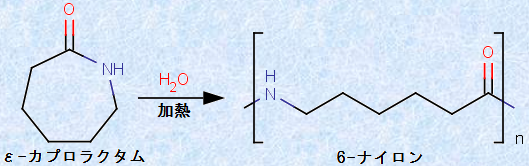
図.8 6-ナイロンの合成反応
ちなみに、「ラクタム(lactam)」というのは、環状のアミド結合(-NHCO-)を持つ物質のことを指します。ε -カプロラクタムという名称は、C6の脂肪酸である「カプロン酸」の「ε位」にアミノ基(-NH2)を持つ「ε -アミノカプロン酸のラクタム」という意味です。置換基の位置番号については、カルボニル基(-CO-)の隣の炭素からα位、β位、γ位、δ位、ε位・・・・・・と呼びます。
(ii) ポリエステル
エステル結合により重合した合成繊維を、「ポリエステル系合成繊維」といいます。主なものに「ポリエチレンテレフタレート(PET)」があり、テレフタル酸とエチレングリコールの縮合重合によって合成される繊維です。1941年にイギリスの化学者であるジョン・ウィンフィールドとジェームズ・ディクソンにより発見されました。発見当初は加工技術などの遅れから、利用は限定的でしたが、1953年にアメリカのデュポン社が特許を取得して、工業化しました。
ポリエチレンテレフタレートは、紫外線を吸収して遮断し、機械的に丈夫で軽量であるという特徴から、溶融加工してペットボトルの原料として大量に利用されています。耐熱性や耐摩耗性に優れ、紫外線にも強いです。また、リサイクルも比較的容易です。ペットボトルの樹脂を細かく砕き、それを加熱して繊維状に紡糸したものが、ワイシャツなどに使われるポリエステル繊維です。ポリエステル系の合成繊維を用いた衣料には、羊毛に近い感触があり、吸湿性がほとんどないため乾き易く、洗濯などによっても型崩れしにくいという特徴があります。ただし、汗を吸収しないので、下着類には不向きであり、染色性がないのが欠点です。また、点火すると融解しながら徐々に燃え、黒褐色の塊を残します。
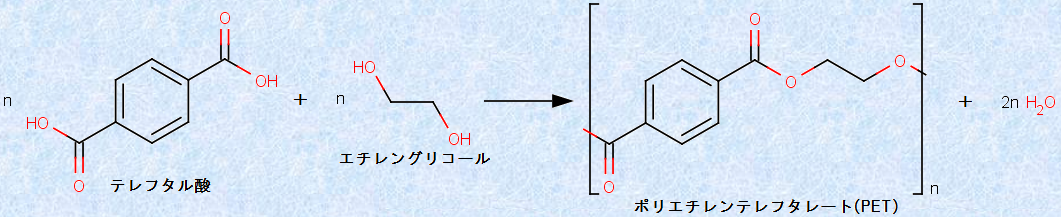
図.9 ポリエチレンテレフタレートの合成反応
(iii) アクリル
主にアクリロニトリルを単量体として付加重合させて作られる合成繊維を、「アクリロニトリル系合成繊維」といい、一般的に「アクリル」と呼ばれています。「ポリアクリロニトリル」は、1950年にアメリカのデュポン社が初めて工業生産を開始し、天然繊維の羊毛に似た風合いを持ち、軽くて保温性に富みます。羊毛の代用品としてセーターや毛布、絨毯などに用いられる他、羊毛や木綿の混紡として、衣料品にも用いられます。アクリル繊維は高温で燃焼させると、有毒なシアン化水素HCNを発生させるので、注意を要します。
また、アクリル繊維を高温で熱処理してできた繊維を「PAN系炭素繊維」といいます。炭素繊維は、重さは鉄Feの1/4であるのに、重量当たりの強さは10倍以上、硬さは7倍にも達します。このように炭素繊維は、軽量・高強度・高弾性で耐熱性に優れるので、釣り竿やゴルフクラブ、飛行機の翼の複合材料などとして用いられます(第14族元素(炭素族元素)を参照)。
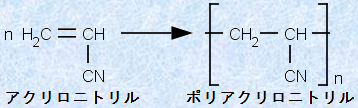
図.10 ポリアクリロニトリルの合成反応
(iv) ビニロン
アメリカのデュポン社が開発したナイロンに衝撃を受けた日本は、日本独自の合成繊維の開発を目指すことにしました。その結果開発されたのが、日本発の合成繊維である「ビニロン」です。まず、酢酸ビニルを付加重合させてポリ酢酸ビニルとし、これをメタノール溶液中で水酸化ナトリウムNaOHなどの塩基で処理すると、加水分解が起こってポリビニルアルコール(PVA)が生じます。ポリビニルアルコールは、形式上はビニルアルコールの付加重合体ですが、ビニルアルコールを付加重合させて合成することはできません。これは、ビニルアルコール自体が極めて不安定な化合物であり、重合させる前に安定なアセトアルデヒドに異性化してしまうためです(脂肪族炭化水素(アルキン)を参照)。そこで、酢酸ビニルを付加重合させ、ポリ酢酸ビニルを合成してから、これを加水分解してポリビニルアルコールを合成するという、回りくどい方法が取られる訳です。
そして、ポリビニルアルコールの親水コロイド溶液を、細孔から飽和硫酸ナトリウムNa2SO4水溶液に押し出すと、塩析が起こって繊維状に固まります。しかし、この状態では、まだ分子中に多くのヒドロキシ基(-OH)があって、水に溶けやすいので、不溶化する必要があります。塩析により凝固させた糸を乾燥後、適当量のホルムアルデヒドHCHOを含む水溶液に1時間ほど浸します。すると、ポリビニルアルコール分子全体の30〜40%のヒドロキシ基(-OH)が、ホルムアルデヒドHCHOのアルデヒド基(-CHO)と付加縮合して、水に不溶の繊維ができあがります。このようにして作る合成繊維を、「ビニロン」といいます。
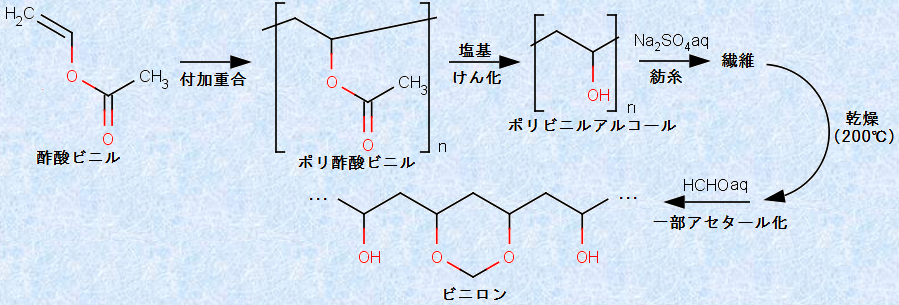
図.11 ビニロンの合成反応
ビニロンには、未反応のヒドロキシ基(-OH)が60〜70%ほど残っているため、水素結合により適度な吸湿性を示し、木綿によく似た性質を示します。合成繊維の中で、吸湿性を持つものは、ビニロン以外にはほとんどありません。ビニロンは、1939年に京都帝国大学(現京都大学)の桜田一郎らによって開発された、日本初の合成繊維です。日本の星野らによる6-ナイロンの開発が1941年ですから、ビニロンはそれよりも2年早い訳です。桜田は、日本の高分子化学の基礎を築いた化学者であり、従来使われていた「高級分子量物質」という言葉に代わって「高分子物質」という日本語を定着させたのも彼です。
ビニロンの開発が発表されると、新聞は「日本のナイロン現る」と書き立てました。戦争の影響で工業化は遅れましたが、1950年には倉敷レイヨン(現在のクラレ)が、世界で初めて工業化に成功しました。合成繊維の中で最も親水性があり、耐摩耗性や耐薬品性に優れているのが特徴です。1960年頃、ビニロンの学生服が大ヒットし、広く一般にビニロンの存在が認知されました。しかし、ゴワゴワとした感触で肌触りがいいとは言えず、徐々に学生服には使われなくなりました。現在では、高強力、高弾性率、親水性、耐薬品性、耐候性などの特性を生かせる方面(防護ネットや帆布、ロープ、漁網、消防服など)に多量に用いられています。

図.12 ビニロンの学生服は人気を博した
(3) プラスチック
合成高分子化合物の多くは、熱や圧力を加えることによって、目的とする形に成形することができます。このような性質を持つ高分子材料を、「プラスチック(plastic)」または「合成樹脂(synthetic)」といいます。「plastic」とは、英語で「自由に成形ができる」という意味です。「樹脂」とは、松脂など木の樹液を乾燥させて得られる固体で、人類が最初に利用したプラスチック様化合物でした。とはいっても、その用途は接着剤や滑り止めなど、限られたものでしかありませんでした。漆も、こうした樹脂の一例に当たります。アジア原産のウルシノキから得られる樹液を、木材などの表面に塗って乾かすと、含まれるウルシオールという成分が、酵素および酸素O2の働きによって、互いに重合して高分子となります。いわば漆器は、プラスチックの遠い祖先に当たるといえるでしょう。

図.13 漆は塗料として用いられ、熱や湿気に強く、腐敗防止、防虫の効果もある
人工的なプラスチックが生まれるのは、19世紀後半になってからのことです。プラスチック第一号のきっかけを作ったのは、スイスの化学者であるフリードリヒ・シェーンバインです。1846年、シェーンバインは硝酸HNO3と硫酸H2SO4の混合液に綿を浸す実験を行いました。そして、その綿にマッチで火を着けた瞬間、綿はパッと燃え上がり、めらめらと鮮やかな無煙の炎をあげ、燃えカスも残さず消えてしまったのです。これは、綿の主成分であるセルロースが、硫酸H2SO4の作用で硝酸HNO3と化合し、ニトロセルロースとなったためです。この化合物は、後に「綿火薬」として、戦場で活躍することになります。
このニトロセルロースに、20%ほどの樟脳を混ぜると硬化することを発見したのは、アメリカの若き発明家ジョン・ウェズリー・ハイエットでした。ハイアットは、1868年にこの新素材を「セルロイド」と名付けて発表しました。そして1870年には、セルロイドを特許化して工業生産を開始しました。自由に成形可能でありながら、硬くて丈夫という性質を持ったセルロイドは、メガネフレームや入れ歯、ピアノの鍵盤、刃物のグリップなどに広く用いられ、爆発的な売れ行きを示しました。これらの商品の多くは、それまで象牙で作られていたので、ハイアットはゾウにとっては大恩人ということになるでしょう。ただし、セルロイドは熱に弱く、非常に燃えやすいという欠点があったため、より扱いやすいプラスチックが出現した現在では、見かける機会が少なくなりました(天然高分子化合物(糖類)を参照)。

図.14 ハイエットは、世界初のプラスチックであるセルロイドを発明したことで知られる
このあと1907年には、アメリカの化学者であるレオ・ベークランドが、フェノールとホルムアルデヒドHCHOを付加縮合させることで、硬い固体を作り出せることを見出し、これを「ベークライト」と名付けて売り出しました。これは、完全な人工合成プラスチックの第一号といわれ、今も電気製品の絶縁体として用いられています。ベークライト(フェノール樹脂)は爆発的な売れ行きを示し、ベークランドは億万長者の1人となりました。そして、1924年9月22日タイム誌の表紙を飾ることになります。

図.15 ベークランドは、ベークライトの工業化に成功し、「プラスチックの父」と呼ばれる
プラスチックの一般的な特徴としては、電気を通さない、耐薬品性がある(分解しにくい)、燃えやすい、紫外線に弱いなどがあげられます。しかし、現在では、電気を通す「導電性プラスチック」や、微生物によって分解される「生分解性プラスチック」、燃えにくい「難燃性プラスチック」など、一般的な性質に当てはまらないプラスチックが製品化されています。プラスチックは、熱に対する性質から、「熱可塑性樹脂(thermoplastic resin)」と「熱硬化性樹脂(thermosetting resin)」に分類されます。
表.2 熱可塑性樹脂と熱硬化性樹脂
|
|
熱可塑性樹脂 |
熱硬化性樹脂 |
|
分子構造 |
長い鎖状構造 |
三次元的な網目状構造 |
|
加工性 |
様々な形に成形しやすい |
複雑な形には成形しにくい |
|
耐熱性 |
弱い |
強い |
|
耐溶剤性 |
弱い |
強い |
(i) 熱可塑性樹脂
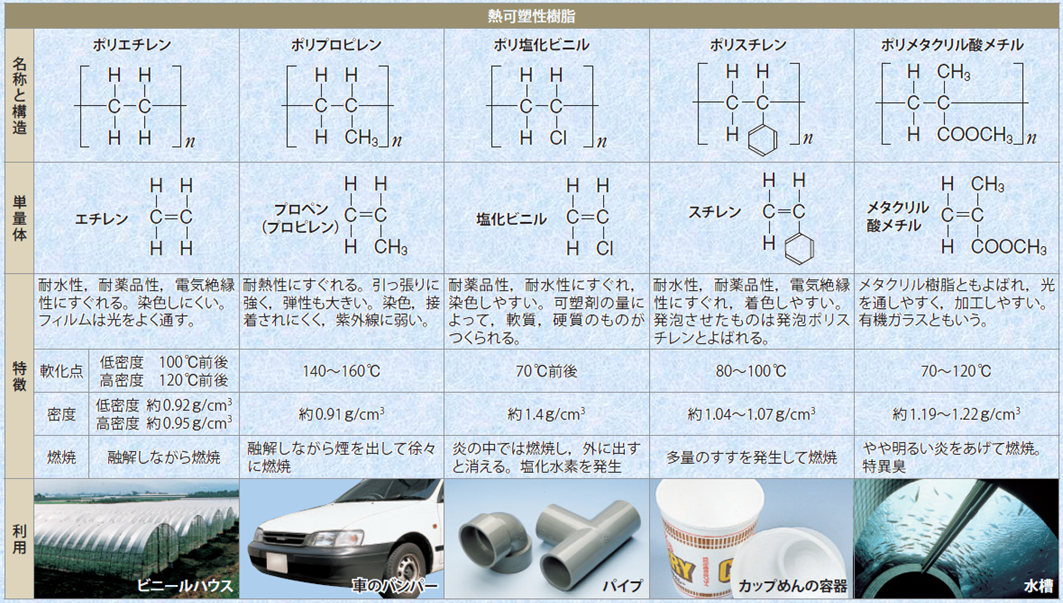
結合手が2本ある分子を多数つなぐと、鎖状の一次元高分子になります。このような高分子を「熱可塑性樹脂」といいます。常温では分子間力で保持されて流動しませんが、熱を加えると軟化し、冷却すると再び硬化する性質を持つプラスチックです。熱可塑性樹脂は、一般的に合成繊維と同様に、鎖状構造を持つ高分子化合物からなり、付加重合で合成されるものが多いです。ただし、ポリエチレンテレフタレート樹脂やナイロン樹脂などは熱可塑性樹脂ですが、縮合重合で合成されています。熱可塑性樹脂は、成形加工が容易であるため、各種シートや包装材料、容器、パイプ、電気絶縁物、歯車、有機ガラスなど、幅広く用いられています。また、成形品だけでなく、適当な有機溶媒を加えて溶かしたものは、接着剤や塗料としても用いられます。次の表.3に、主な「熱可塑性樹脂」とその用途を示します。
表.3 主な熱可塑性樹脂とその用途
(ii) 熱硬化性樹脂
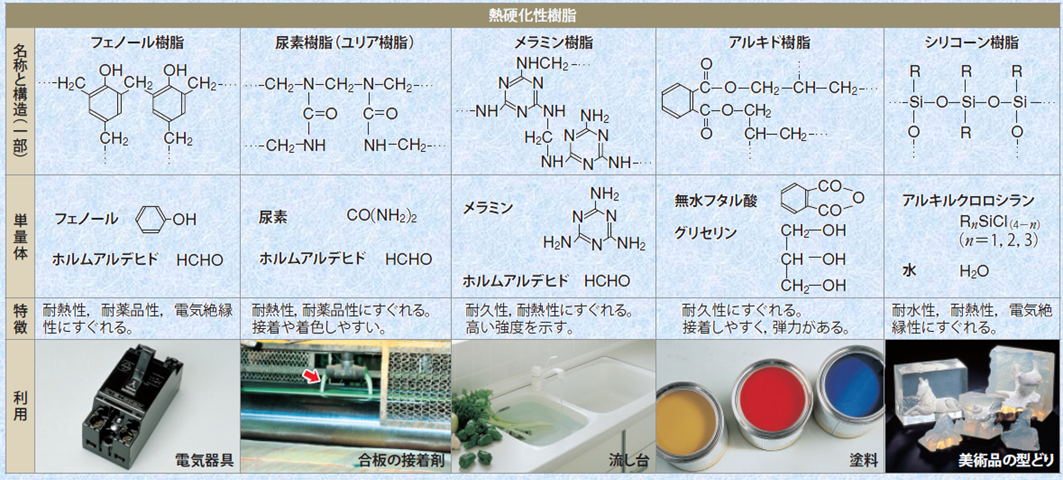
結合手が3本以上ある分子を多数つなぐと、必ず環状構造ができ、三次元網目状高分子になります。このような高分子を「熱硬化性樹脂」といいます。加熱することで硬化反応が進行し、熱や溶剤に強くなる性質を持ちます。熱可塑性樹脂と違って、一度硬化したあとは、再び熱を加えても軟らかくなりません。熱硬化性樹脂は、付加反応と縮合反応の繰り返しで起こる重合反応である「付加縮合(addition condensation)」で合成されるものが多く、合成過程の熱処理で重合反応が進み、三次元網目状構造が発達して、硬くなります。一般的には熱処理だけでなく、硬化剤や補強材を加えて熱処理されることが多いです。熱硬化性樹脂は、熱可塑性樹脂と比較すると、機械的強度や耐熱性、耐薬品性などに優れるため、電気器具やテーブル、棚、食器、雑貨、塗料など幅広く利用されています。
表.4 主な熱硬化性樹脂とその用途
(ii-1) フェノール樹脂
「フェノール樹脂」は、フェノールとホルムアルデヒドHCHOを付加縮合させることで作られる合成樹脂です。フェノール樹脂は、アメリカの化学者であるレオ・ベークランドが1907年に発明した、世界初の完全な合成樹脂です。発明者であるベークランドの名にちなんで、「ベークライト」とも呼ばれます。電気産業が発達しつつあった当時、強度が高く優れた電気絶縁性を持つフェノール樹脂は、電気部品やプリント電子配線基板などの電気絶縁材料として世の中に急速に普及し、爆発的な売れ行きを示しました。当時の絶縁体の製造は、「ラックカイガラムシ」という東南アジア原産の虫が分泌する「シェラック」という樹脂に頼っており、450 gのシェラックを作るのに15,000匹ものラックカイガラムシと半年もの期間が必要でした。当時のアメリカは、年間数千トンものシェラックを輸入していたので、安価なフェノール樹脂の登場は業界に衝撃を与えました。1978年には、ベークランドは全米発明家殿堂入りを果たしています。

図.16 ラックカイガラムシ(左)とシェラック(右)
フェノール樹脂は、合成時の触媒が、酸であるか塩基であるかにより反応が若干異なり、用途により触媒が選択されます。希硫酸H2SO4などを用いて酸触媒下で合成を行うと、付加縮合反応が起こって、分子量が1,000程度の「ノボラック」と呼ばれる熱可塑性樹脂が得られます。ノボラックは、一般的に軟らかい固形の樹脂であり、ノボラックは加熱しても硬化しないため、硬化させて使用する場合には、硬化剤を加えて加熱する必要があります。
また、水酸化ナトリウムNaOHなどを用いて塩基触媒下で合成を行うと、付加反応が起こりやすくなって、分子量が500以下の「レゾール」と呼ばれる熱硬化性樹脂が得られます。レゾールは、一般的に粘性の大きな液状であることが多く、ヒドロキシメチル基(-CH2OH)を多く有するため、そのまま加熱するだけで硬化させることができます。
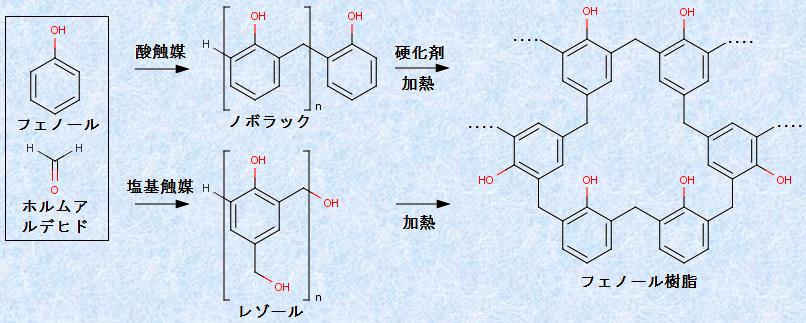
図.17 フェノール樹脂の合成反応
(ii-2) 尿素樹脂
アミノ基(-NH2)を持つ化合物と、ホルムアルデヒドHCHOを付加縮合させて作る熱硬化性樹脂を、「アミノ樹脂」といいます。代表的なアミノ樹脂が、「尿素樹脂(ユリア樹脂)」です。まず、尿素(NH2)2COとホルムアルデヒドHCHOを塩基性条件で反応させ、低分子のプレポリマーを作ります。このプレポリマーは粘性の大きな無色透明の液体で、ベニヤ板などの接着剤にも使われています。そして、このプレポリマーに充填剤や着色剤を加え、酸性条件で加熱すると、付加縮合が進行して尿素樹脂ができます。
尿素樹脂は、無色透明で着色や成型がしやすく、耐熱性や電気絶縁性が高いという特徴があり、食器や照明器具、キャビネット、ボタン、化粧板などに用いられています。尿素樹脂は、文房具やおもちゃの他、食器にも使用されているので、名称に「尿素」という語は、語感があまり良くないということで、もっぱら「ユリア樹脂」という名称が、好まれて使われています。ただし、「ユリア」という名称の方も、英語で「尿素」を意味する「urea」の訛りであるから、結局は同じことではありますが。
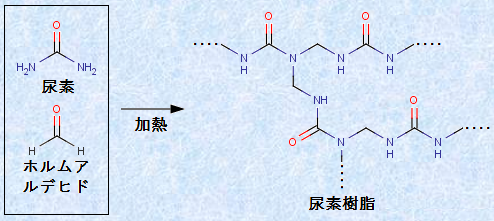
図.18 尿素樹脂の合成反応
(ii-3) メラミン樹脂
「メラミン樹脂」は、メラミンとホルムアルデヒドHCHOから作られるアミノ樹脂で、尿素樹脂と同様の方法で合成されます。メラミン樹脂は、合成樹脂中で最高の強度や耐衝撃性を持ちます。さらに、表面は美しい光沢を持ち、耐水性や耐候性、耐摩耗性にも優れているため、家具や木工製品の表面材の接着、あるいは食器や実験室のテーブルなどに利用されることが多いです。
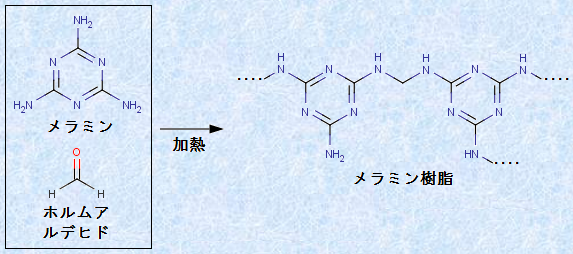
図.19 メラミン樹脂の合成反応
「メラミン」と聞くと、2007年に中国企業が起こした事件を思い出す人もいるかもしれません。タンパク質に含まれている窒素NをアンモニアNH3に変化させて、タンパク質を定量する方法を「ケルダール法(Kjeldahl method)」といいます。食品中のタンパク質含有量を調べる一般的な方法です。この手法を逆手に取り、ペットフードや粉ミルクなどに窒素含有率の高いメラミンを混入させ、タンパク質含有量を偽装する事件が起こりました。この事件により、アメリカの犬や猫、中国の幼児が腎不全を引き起こし、世界的な大問題となりました。化学の知識をこのように悪用する者がいるのは、実に残念なことです。
(ii-4) シリコーン樹脂
ジクロロジメチルシラン(CH3)2SiCl2やトリクロロメチルシランCH3SiCl3は、水H2Oと容易に反応し、それぞれジメチルシラノール(CH3)2Si(OH)2やメチルシラノールCH3Si(OH)3になります。これらのシラノールが縮合重合し、三次元的網目状構造を持つ樹脂を、「シリコーン樹脂(ケイ素樹脂)」といいます。「シリコーン(silicone)」というのは、「シリコン(silicon)」とケトン(ketone)の語尾「one」をつなげて命名したものです。しかし、ケトンのC=O結合のようにSi=O結合は通常存在せず、ケイ素Siと酸素Oが交互に長くつながった構造をしています。
シリコーン樹脂は、無機高分子化合物の1つであり、化学的に安定で、耐熱性や耐水性に優れます。その表面に撥水性を持ち、電気絶縁性もあります。分子の長さによって粘度も調節できるため、グリースやブレーキオイル、コンタクトレンズやシャンプーなど、身の回りで広く利用されています。
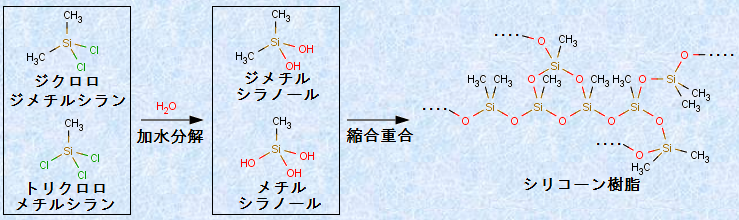
図.20 シリコーン樹脂の合成反応
(4) ゴム
小さな力で、大きな伸び縮みをする性質を「ゴム弾性(rubber elasticity)」といい、このような性質を持つ高分子化合物を、「ゴム(rubber)」といいます。ゴムは、現代科学技術において必須の製品です。多くの産業に必要な水道やガスなどは、パイプの接続部分から漏れないことが前提として整備されています。そして、それはゴムによって密閉されているのです。ゴムには、ゴム製品とその材料としての原料ゴムがあり、さらに原料ゴムは、「天然ゴム(natural rubber)」と「合成ゴム(synthetic rubber)」に分類されます。この実用的なゴムの製造法を発明したのは一人のアメリカ人で、まさにゴムに憑りつかれた男でした。
(i) 天然ゴム
ゴム園は、そのほとんどが赤道周辺、特に東南アジア諸国に集中しています。中南米原産のクワ科の植物であるゴムの木の幹に傷を付けると、そこから白い粘性のある樹液が染み出してきます。これを何千本もの樹木から集めるという、非常に地道な作業をします。こうして得られた白い乳液を、「ラテックス(latex)」といいます。ラテックスは、直径500 nm程度の微細なゴムの粒子が、表面にあるタンパク質の保護作用によって、水に分散した疎水コロイド溶液です。これに凝固剤として有機酸(ギ酸HCOOHや酢酸CH3COOHなど)を加えて凝析させたものを、「天然ゴム」または「生ゴム」といいます。なお、凝析の際に塩酸HClを用いることはできません。塩酸HClは、ゴム分子中の二重結合へ付加する副反応を起こすからです。
ちなみに、ラテックスが何のために分泌されているのか、明確には分かっていません。しかし、ゴムの木以外にも、ラテックスを分泌する植物は他にもいくつかあり、代表的なものがタンポポです。タンポポの葉や茎を切ったときに出る白い液体がラテックスです。過去には、タンポポのラテックスによるゴムが製造されていたこともありました。また、メキシコには、「サポディラ」という木があり、原住民たちは、その樹液から得られる「チクル」を噛む習慣がありました。これが、現在のチューイングガムの起源とされています。しかし、ラテックスの供給源として最も優れているのは、やはりゴムの木です。ゴムの木の幹に傷を入れて、そこからしたたる樹液を集めて凝固させるだけで、簡単にゴムが得られます。

図.21 ラテックスは、タンパク質やアルカロイド、タンニン、天然ゴムなどが分散した疎水コロイドである
天然ゴムは、「イソプレン(2-メチル-1,3-ブタジエン)C5H8」という分子が付加重合した構造を持つ、「シス形ポリイソプレン」です。天然ゴムを乾留すると、イソプレンC5H8という化合物のみが生成物として得られることから、その化学構造が決定されました。イソプレンC5H8は、CH2=CH-C(CH3)=CH2の示性式で表されるジエン系の炭化水素で、単結合を間に挟んだ二重結合(このような二重結合を「共役二重結合(conjugated double bond)」といいます)を持つ化合物です。共役二重結合を持つ単量体を付加重合させると、分子中に二重結合を残した重合体ができます。
天然ゴムは、力が加わっていないときは、ポリイソプレン分子が「シス形」であるため、分子全体が曲がりくねった丸まった形をしています。そのため、ゴム分子鎖の間には、比較的多くの隙間が生じ、分子間力があまり強く作用しません。したがって、ほとんど結晶化は起こらず、軟らかな物質となります。ゴム分子を引っ張ると、主鎖中の炭素原子間の単結合(-CH2-CH2-)がそれを軸として回転できることから、分子全体が伸びて、分子の配列が規則正しい形になります。しかし、引っ張るのを止めると、伸びた分子はこの状態がエントロピー的に不安定なため、-CH2-CH2-の炭素間結合を軸にして回転し、元のように丸まった乱雑な状態に戻ろうとします。このような理由で、ゴムは特有の弾性を示すのです。ゴムのように外力を加えたときのエントロピーの小さい状態から、元のエントロピーの大きな乱雑な状態に戻ろうとして生じる弾性を、「エントロピー弾性(entropy elasticity)」といいます。
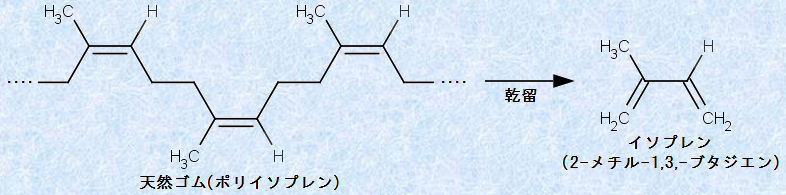
図.22 天然ゴムを乾留すると、イソプレンC5H8が得られる
また、天然ゴムの単量体である「イソプレンC5H8」という分子は、自然界に存在する物質の重要な単位構造であり、多くの化合物が、このイソプレンC5H8を基礎として作られています。例えば、柑橘類の香り成分である「リモネンC10H16」やミントの香り成分である「メントールC10H20O」は2つのイソプレン単位、バラの香り成分である「ファルネソールC15H26O」は3つのイソプレン単位、ニンジンの色素である「カロテンC40H56」は8つのイソプレン単位を元にして作られています。レモンやバラの香り成分とゴムは、一見すると似ても似つきませんが、分子レベルで見れば、非常に近い親戚筋ということになります。
イソプレンC5H8が単位構造であるという証拠は、簡単な実験で確かめられます。膨らませたゴム風船に、レモンの皮の搾り汁をかけるのです。しばらくすると、風船は破裂してしまいます。似た性質を持つ分子は混じり合いやすいので、皮に含まれるリモネンがゴムの成分を溶かし、風船の膜を弱めて、破裂させてしまうのです。
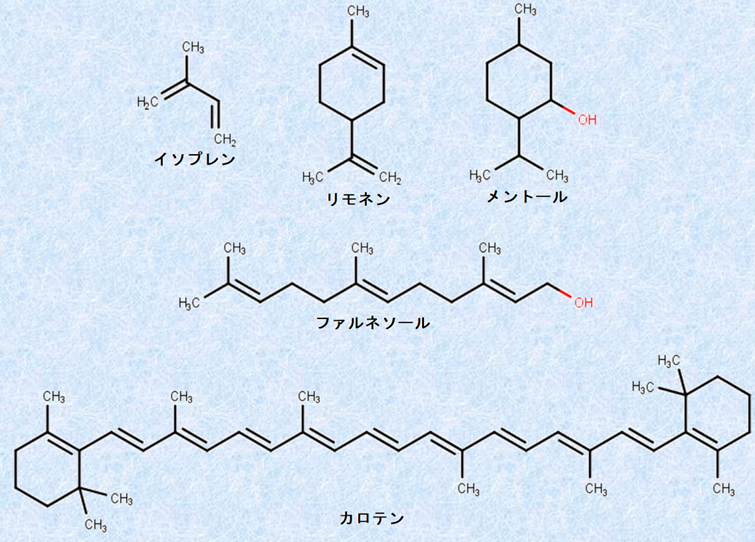
図.23 多くの化合物が、イソプレンC5H8を単位構造としている
また、マレー語で「ゴムの木」という意味の「ガタパーチャ」といわれるマレーシア原産のアカテツ科の樹木から得られる樹脂は、「トランス形ポリイソプレン」だけでできています。トランス形ポリイソプレンは、分子鎖が真っすぐに伸びた構造を取りやすく、分子鎖がより近くまで接近できます。したがって、分子間力が強く作用して、結晶化しやすくなります。ガタパーチャから得られる天然ゴムは、通常の天然ゴムより固く強靭で、ゴム弾性に乏しいです。そのため、この天然ゴムは、ゴルフボールの外皮や歯科用充填剤に利用されています。

図.24 ガタパーチャはトランス形ポリイソプレンで、適度な強靭さがあるため、ゴルフボールの外皮に用いられる
天然ゴムの分子は長い鎖状で、二重結合がいくつもあります。空気中では、この部分が酸素O2やオゾンO3によってゆっくり酸化され、構造が変化するため、次第にゴム弾性を失って劣化します。さらに、天然ゴムの分子は、長い鎖同士が弱いファンデルワールス力で引き合っているだけなので、温度が上がると分子の熱運動が激しくなり、軟らかくなってしまうという欠点がありました。19世紀前半までのゴム製品は、温度に非常に影響されやすく、冬には低温でカチカチに固まり、夏には熱でベトベトに溶けるような代物でした。そのため、当時のゴム製品を販売する会社は、製品の信頼性の不足のために、倒産寸前の会社が多かったといいます。
1834年、当時34歳だったアメリカの発明家チャールズ・グットイヤーは、当時の不完全なゴムの性質を、何とかしようと決心しました。グットイヤーは、ゴムが溶解するのは湿気のせいと考え、乾燥した粉末を混ぜれば、これを克服できるというアイディアを持っていました。しかし、実験はなかなか上手くいかず、資金を失って設備を売り払ったため、友人の屋根裏部屋で実験をすることもありました。ときには、実験中に発生した有毒ガスで中毒になり、危うく死にかけたこともあったといいます。グットイヤーは実験を続けるため、家財道具のほとんどを売り払い、子供の学校の教科書を質屋に入れるほど困窮していました。所用でボストンに行ったときは、ホテル代の5ドルを払えずに、拘留されました。
しかし、真摯なグットイヤーを、神は見放しませんでした。1839年の冬、グットイヤーは実験で天然ゴムに硫黄Sを少量混ぜ、それを加熱することで、強い弾性と耐久性を持たせられること(加硫法)を発見したのです。この発見により、ゴムの性質が飛躍的に向上し、ゴムは夏でも冬でも使えるようになりました。グッドイヤーは早速特許を取得し、1842年にゴム工場を立ち上げました。そして、グッドイヤーはこの功績を称えられ、1976年には、オハイオ州アクロンの「発明者の殿堂」にノミネートされました。

図.25 グットイヤーは、幾多の苦難を乗り越え、天然ゴムに硫黄Sを混ぜる方法を発見した
なお、世界的なタイヤ製造会社であるグットイヤー社は、彼の名にちなんで命名されていますが、グットイヤー本人やその一族とは、法的・資本的な関係はありません。実のところ、グッドイヤーは画期的な発明は成し遂げたものの、事業家としては、全く成功できませんでした。グッドイヤーの特許は、あちこちで侵害を受け、グッドイヤーは多数の裁判を闘う羽目となりました。特にイギリスでは、特許をまるまる他人に奪われました。グッドイヤーが売り込みのため、製法を明らかにせずにサンプルを送ったところ、受け取ったゴム会社はこれを分析して、表面にわずかな硫黄Sが付着していることを見つけます。この企業は、早速同じような特許を申請し、こちらが成立してしまったのです。結局、グッドイヤーは巨額な借金を抱えたまま、自らの発明が世界を変えていく様を見ることもできず、1860年に世を去っています。彼の名にちなんだグットイヤー社の設立は、それから38年後の1898年です。

図.26 グットイヤー社は世界的なタイヤ製造会社である
天然ゴムに硫黄Sを5〜8%程度加えて、140℃程度に加熱するという単純な操作で、それまで温度変化に弱かったゴムは、非常に安定した物質に化けました。これは、硫黄Sが鎖状のゴム分子に残っている二重結合部分をところどころで架橋して、ゴム分子同士を結合させたからです。このように架橋構造を作る操作を「加硫(vulcanization)」といい、このとき生じたゴムを「弾性ゴム」、または「加硫ゴム」といいます。加硫ゴムは、ゴム弾性や機械的強度が大きいだけでなく、石油などにも溶けにくく、酸素O2やオゾンO3によっても酸化されにくいです。このように、加硫ゴムはすべての面において、天然ゴムよりも優れた性質を持ちます。
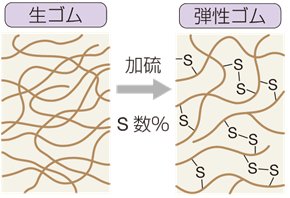
図.27 加硫と弾性ゴム
さらに、天然ゴムに30〜40%の硫黄Sを加えて、長時間加熱すると、「エボナイト」という黒色の硬い物質にもなります。この物質を発見したのは、グッドイヤーの弟であるネルソン・グッドイヤーです。「エボナイト」とは、古代から世界各国で家具や弦楽器などに使用される熱帯性常緑高木の「エボニー(黒檀)」に似ていることから名付けられました。エボナイトは、酸や塩基などに強く、機械的強度が高いため、ボウリングの球や万年筆の軸、マウスピースなどに用いられています。噛んだときに他のプラスチックのような「カチン」とした不快感が少ないため、管楽器の吹き口などにも用いられます。なお、エボナイトの見た目や質感はプラスチックに似ていますが、エボナイトは飽くまでゴムの一種であり、天然樹脂に分類されるものです。

図.28 エボナイトは、見た目や質感はプラスチックと似ているが、飽くまでゴムの一種である
ちなみに、「ゴム」という素材をヨーロッパに初めてもたらしたのは、クリストファー・コロンブスの艦隊だといわれています。1493年の第二回目の航海で、プエルトリコとジャマイカに上陸し、そこで原住民が大きく跳ねるボールで遊んでいるのを見て、とても驚いたそうです。しかし、持ち帰られたゴムは、文字消しやおもちゃとして使われただけでした。当時は、「加硫」という操作がまだ知られておらず、ゴムは冬にはカチカチに固まり、夏には溶けてベタベタになるような代物であったからです。ゴムが広く用いられるようになるには、「加硫」という大きなブレイクスルーが必要でした。ちなみに、ゴムを意味する「ラバー(rubber)」は、英語で「こすって消す(rub out)」、つまり「文字消し」から来ています。消しゴムが開発される以前は、湿った食パンで文字を消していたといいます。
(ii) 合成ゴム
イソプレンC5H8や、イソプレンC5H8に似た構造を持つ単量体を付加重合させると、天然ゴムによく似た性質を持つ物質が得られます。このような物質を「合成ゴム(synthetic rubber)」といい、戦争による天然ゴムの供給不足を補うために、まず1914年にドイツで、次いでアメリカで合成ゴムの開発が始まりました。第二次世界大戦後には、天然ゴムにはない新しい特性を持った合成ゴムが生産されるようになりました。現在、使用されているゴムの約3/4は合成ゴムが占めています。合成ゴムは、生分解性で天然ゴムに劣りますが、天然ゴムよりも耐油性や耐老化性、耐摩耗性、耐熱性などに優れたものを作ることができるため、用途に応じて様々なものがあります。
例えば、1,3-ブタジエンやクロロプレンを付加重合させると、これらの単量体分子の中央部に二重結合が移動して、分子の両端で1,4付加し、「ブタジエンゴム(BR)」や「クロロプレンゴム(CR)」ができます。付加するときに二重結合の位置が変わるのは、これら合成ゴムの単量体が、共役した二重結合を持っているからです。ブタジエンゴムは、弾性や耐摩耗性、耐寒性に優れ、タイヤやゴムホース、ゴルフボール、スーパーボールなどに用いられます。他種のゴムと混合して用いることも多く、汎用合成ゴムの1つです。クロロプレンゴムは、耐熱性や耐油性、耐薬品性は天然ゴムよりも優れ、加工も容易であるため、コンベヤベルトやウェットスーツなどに使用されます。
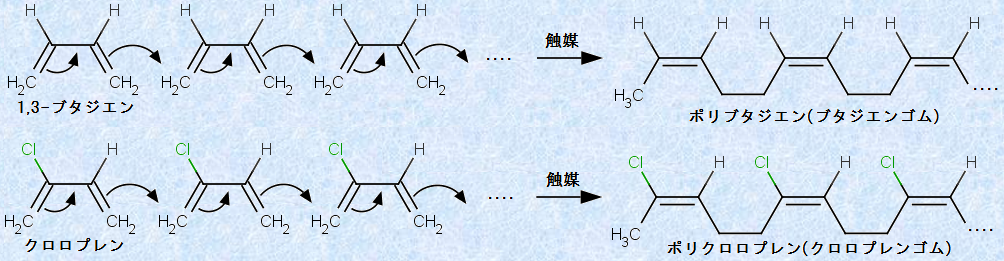
図.29 ブタジエンゴムとクロロプレンゴムの合成反応
また、共重合で生じる合成ゴムもあり、1,3-ブタジエンにスチレンを20〜25%ほど混合し、適当な触媒を用いて共重合させると、「スチレン-ブタジエンゴム(SBR)」ができます。スチレン-ブタジエンゴムは、分子中にベンゼン環が入ったことにより、耐老化性や耐熱性、耐水性、耐摩耗性、機械的強度に優れ、品質が安定して良好な加工性を示すため、自動車用タイヤ材として最もよく使用されます。スチレン-ブタジエンゴムは、生産されてる合成ゴム中の約60%を占め、最も使用量が多い合成ゴムです。
ちなみに、自動車で使われるタイヤには、スタッドレスタイヤとノーマルタイヤがあります。見た目には、大きな違いがあるように思えませんが、一体どこが違うのでしょうか。大きく異なる点は、使われているゴムの質にあります。一般的にゴムは、温度が下がると、ゴム弾性を失って硬くなります。しかし、スタッドレスタイヤは、温度が下がっても、ゴム弾性を失わないようになっているのです。さらに、スタッドレスタイヤには、「ミウラ折り」などの工夫をした特殊なトレッドパターンが採用されており、滑りの原因となる氷上の水膜を、走行中に効率的に除去できるようになっています。
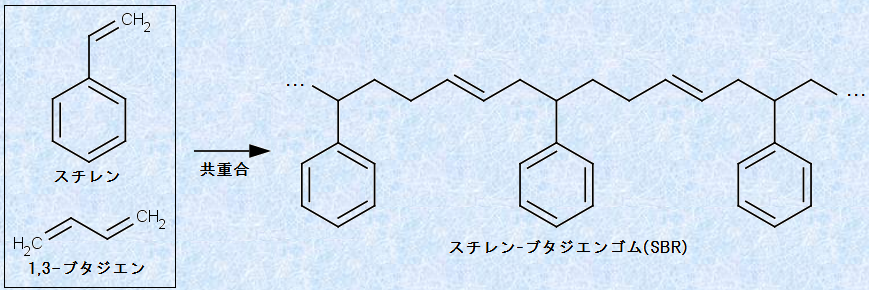
図.30 スチレン-ブタジエンゴムの合成反応
さらに、ブタジエン骨格を含まないゴムもあり、「シリコーンゴム」がそれです。シリコーンゴムは、分子内に炭素-炭素二重結合を持たないため、長時間空気にさらしても酸化されにくく、劣化しにくいという特徴を持ちます。なお、「シリコン」は、単体のケイ素(silicon)の元素を表しますが、ケイ素の合成高分子化合物は、「シリコーン(silicone)」と伸ばすのが正しい表記です。よく用いられる「シリコンゴム」というのは、誤った表現なので注意してください。シリコーンゴムは、塩基を触媒として、ジクロロジメチルシランを加水分解して得られます。比較的高価ではありますが、耐熱性や耐寒性、耐薬品性、電気絶縁性に優れているので、理化学器具やパッキング材料などに用いられます。また、生体に対する影響が少ないので、人工血管などの医療器具にも用いられます。
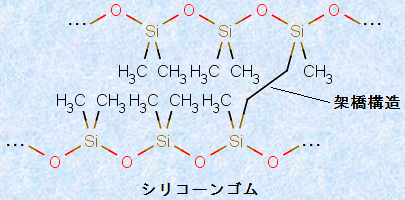
図.31 シリコーンゴムの構造
・参考文献
1) 大東孝司「プラグマティック化学」河合出版(2017年発行)
2) 齊藤烈/藤嶋昭/山本隆一/他19名「化学基礎」啓林館(2012年発行)
3) 佐藤健太郎「世界史を変えた新素材」新潮社(2018年発行)
4) 左巻健男「面白くて眠れなくなる化学」PHP研究所(2012年発行)
5) 左巻健男「絶対に面白い化学入門 世界史は化学でできている」ダイヤモンド社(2021年発行)
6) H.ハート/L.E.クレーン/D.J.ハート 共著「ハート基礎有機化学」培風館(1986年発行)
7) 船山信次「こわくない有機化合物超入門」技術評論社(2014年発行)
8) 古川安「カロザースとナイロン―伝説再考」化学と教育55巻6号(2007年)