پEژ‰–b‘°’Y‰»گ…‘f(ƒAƒ‹ƒPƒ“)
پy–عژںپz
(i) ƒnƒچƒQƒ“‚ج•t‰ء(ƒnƒچƒQƒ“‰»)
(vi) ‰كƒ}ƒ“ƒKƒ“ژ_ƒCƒIƒ“‚ة‚و‚éژ_‰»
(i) گA•¨ƒzƒ‹ƒ‚ƒ“‚ئ‚µ‚ؤ“‚ƒGƒ`ƒŒƒ“
(1) ƒAƒ‹ƒPƒ“
ƒGƒ`ƒŒƒ“CH2پپCH2‚âƒvƒچƒsƒŒƒ“CH2پپCHCH3‚ب‚ا‚ج•ھژq‚حپA•ھژq’†‚ج’Y‘fŒ´ژqٹش‚ة’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚ً1‚آٹـ‚فپA‘¼‚ح‚·‚ׂؤ’PŒ‹چ‡‚إ‚·پB‚±‚ج‚و‚¤‚بچ½ژ®’Y‰»گ…‘f‚ًپAˆê”ت“I‚ةپuƒAƒ‹ƒPƒ“(alkene)پv‚ئ‚¢‚¢‚ـ‚·پB‚·‚ׂؤ‚جƒAƒ‹ƒPƒ“‚حپAˆê”تژ®CnH2n(nپ†2)‚إ•\‚³‚ê‚ـ‚·پBƒAƒ‹ƒPƒ“‚حپu•s–Oکa(unsaturated)‚إ‚ ‚éپv‚ئ‚¢‚ي‚ê‚ـ‚·‚ھپA‚±‚ج——R‚حپAƒAƒ‹ƒJƒ“CnH2n+2‚ة”ن‚ׂؤپA’Y‘fگ”‚ة‘خ‚·‚éگ…‘fگ”‚ھڈ‚ب‚¢‚©‚ç‚إ‚·پB1 mol‚جƒAƒ‹ƒPƒ“CnH2n‚ة1 mol‚جگ…‘fH2‚ً•t‰ء‚³‚¹‚é‚ئپA1 mol‚جƒAƒ‹ƒJƒ“CnH2n+2‚ھگ¶گ¬‚µ‚ـ‚·پB
CH2پپCH2پ@پ{پ@H2پ@پ¨پ@CH3CH3
•s–Oکa’Y‰»گ…‘f‚ج’†‚ة‚حپA“ٌڈdŒ‹چ‡‚ً2Œآˆبڈمژ‚آ‰»چ‡•¨‚à‘¶چف‚µ‚ـ‚·پB2Œآ‚ج“ٌڈdŒ‹چ‡‚ًژ‚آ‰»چ‡•¨‚حپuƒAƒ‹ƒJƒWƒGƒ“(alkadiene)پv‚إ‚ ‚èپAˆê”ت“I‚ة‚حپuƒWƒGƒ“(diene)پv‚ئŒؤ‚خ‚ê‚ـ‚·پB“ٌڈdŒ‹چ‡‚ً3Œآژ‚آپuƒgƒٹƒGƒ“(triene)پvپA“ٌڈdŒ‹چ‡‚ً4Œآژ‚آپuƒeƒgƒ‰ƒGƒ“(tetraene)پvپA‚»‚µ‚ؤ“ٌڈdŒ‹چ‡‚ًگ”‘½‚ژ‚آپuƒ|ƒٹƒGƒ“(polyene)پv‚à‚ـ‚½‘¶چف‚µ‚ـ‚·پB
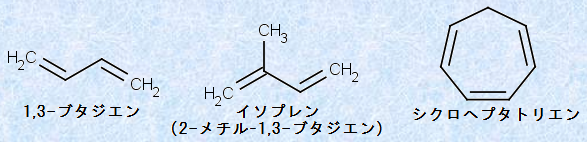
گ}.1 “ٌڈdŒ‹چ‡‚ً2Œآˆبڈمژ‚آ—lپX‚ب‰»چ‡•¨
(i) “ٌڈdŒ‹چ‡‚ج“ء’¥
’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚ة‚حپA’PŒ‹چ‡‚ئ‚حˆظ‚ب‚é‚¢‚‚آ‚©‚ج“ء’¥‚ھ‚ ‚è‚ـ‚·پB—ل‚¦‚خپA“ٌڈdŒ‹چ‡‚ًچ\گ¬‚·‚éٹe’Y‘fŒ´ژq‚حپA‘¼‚ة3Œآ‚جŒ´ژq‚ئ‚µ‚©Œ‹چ‡‚µ‚ـ‚¹‚ٌپB‚³‚ç‚ةپAƒAƒ‹ƒPƒ“•ھژq‚إ‚حپA“ٌڈdŒ‹چ‡‚إŒ‹‚ر‚آ‚¢‚ؤ‚¢‚é’Y‘fŒ´ژq2Œآ‚ئپA‚±‚ê‚ç‚ج’Y‘fŒ´ژq‚ةŒ‹‚ر‚آ‚¢‚ؤ‚¢‚錴ژq4Œآ‚جŒv6Œآ‚جŒ´ژq‚ھپA“¯ˆê•½–ت‚ةŒإ’肳‚ê‚ؤ‚¢‚ـ‚·پBژں‚جگ}.2‚ةپAƒGƒ`ƒŒƒ“CH2پپCH2‚ة‚آ‚¢‚ؤ‚±‚ج•½–تگ«‚ًژ¦‚µ‚ـ‚·پB
گ}.2 ƒGƒ`ƒŒƒ“CH2پپCH2‚ج•½–تگ«
ƒGƒ`ƒŒƒ“‚جH-C-H‚¨‚و‚رH-CپپCٹp‚حپA‚ظ‚ع120پ‹‚إ‚·پB’PŒ‹چ‡(ƒذŒ‹چ‡)‚ج‚ـ‚ي‚è‚ج‰ٌ“]‚حژ©—R‚ة‹N‚±‚è‚ـ‚·‚ھپA“ٌڈdŒ‹چ‡‚ج‚ـ‚ي‚è‚ج‰ٌ“]‚ح‘©”›‚³‚ê‚ؤ‚¢‚ـ‚·پB‚آ‚ـ‚èپA2Œآ‚جگ…‘f‚ئŒ‹چ‡‚µ‚ؤ‚¢‚é’Y‘fŒ´ژq‚حپA‘¼•û‚ج’Y‘f‚ة‘خ‚µ‚ؤپA‰ٌ“]‚·‚邱‚ئ‚ح‚ ‚è‚ـ‚¹‚ٌپB‚³‚ç‚ةپA’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚حپA’Y‘f-’Y‘f’PŒ‹چ‡‚و‚è’Z‚¢‚±‚ئ‚à“ء’¥“I‚إ‚·پB‚±‚ج‚و‚¤‚ب’PŒ‹چ‡‚ئ“ٌڈdŒ‹چ‡‚ج‘ٹˆل“_‚ًپAژں‚ج•\.1‚ةژ¦‚µ‚ـ‚·پB
•\.1 ’Y‘f-’Y‘f’PŒ‹چ‡‚¨‚و‚ر’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚ج”نٹr
|
|
’Y‘f-’Y‘f’PŒ‹چ‡ |
’Y‘f-’Y‘f“ٌڈdŒ‹چ‡ |
|
’Y‘f‚جŒ´ژq‰؟ |
4(گ³ژl–ت‘جŒ`) |
3(•½–تژO•ûŒ`) |
|
‰ٌ“] |
”نٹr“Iژ©—R |
‘©”›‚³‚ê‚ؤ‚¢‚é |
|
—§‘جچ\‘¢ |
‘½گ”‚ج”zچہ‚ھ‰آ”\ |
•½–ت |
|
Œ‹چ‡ٹp |
109.5پ‹ |
120پ‹ |
|
Œ‹چ‡‹——£ |
0.154 nm |
0.134 nm |
“ٌڈdŒ‹چ‡‚ًچ\گ¬‚·‚é’Y‘fŒ´ژq‚ھپA‚±‚ج‚و‚¤‚بگ«ژ؟‚ًژ¦‚·‚ج‚حپA’Y‘fŒ´ژq‚ھپAژ©گg‚ج2sپE2pxپE2py‹O“¹‚ً‘g‚فچ‡‚ي‚¹‚ؤپA3‚آ‚جگV‚µ‚¢پusp2چ¬گ¬‹O“¹پv‚ًچى‚ء‚ؤ‚¢‚é‚©‚ç‚إ‚·پBژں‚جگ}.3‚ة‚حپA’Y‘fŒ´ژq‚ھsp2چ¬گ¬‹O“¹‚ًŒ`گ¬‚·‚é—lژq‚ھژ¦‚µ‚ؤ‚ ‚è‚ـ‚·پB‚ب‚¨پAچ¬گ¬‚ةژg‚ي‚ê‚ب‚©‚ء‚½2pz‹O“¹‚حپA–¢چ¬گ¬‚ج‚ـ‚ـژc‚ء‚ؤ‚¢‚ـ‚·پBsp2چ¬گ¬‹O“¹‚إ‚حپA’PŒ‹چ‡(ƒذŒ‹چ‡)‚ةٹض—^‚·‚é“™‚µ‚¢ƒGƒlƒ‹ƒMپ[ڈ€ˆت‚ج‹O“¹‚ھ3‚آ‚ ‚èپA‚±‚ê‚ç‚ھ‘¼‚ج‹O“¹‚ئڈd‚ب‚èچ‡‚¤‚±‚ئ‚إپA3‚آ‚جƒذŒ‹چ‡‚ًŒ`گ¬‚µ‚ـ‚·(ڈعچׂحچ¬گ¬‹O“¹‚ًژQڈئ)پB
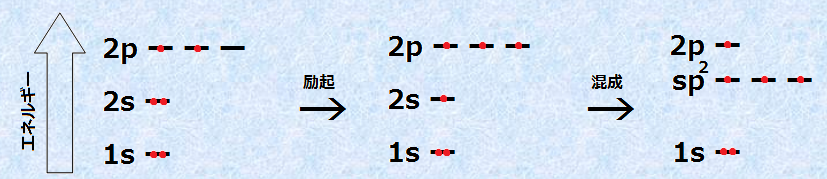
گ}.3 ’Y‘f‚جsp2چ¬گ¬‹O“¹
ƒذŒ‹چ‡‚ًŒ`گ¬‚·‚ésp2چ¬گ¬‹O“¹‚حپAٹe‹O“¹ٹش‚ج“dژq‚ج”½”‚ًچإڈ¬‚ة‚·‚邽‚كپAٹe‹O“¹ٹش‚جٹp“x‚ً120پ‹‚ة‚µ‚ـ‚·پB‚±‚ê‚ة‚و‚ء‚ؤپAٹe‹O“¹‚حپA‘¼‚ج‹O“¹‚©‚ç‚إ‚«‚邾‚¯—£‚ꂽˆت’u‚إ‘¶چف‚إ‚«‚é‚و‚¤‚ة‚ب‚é‚ج‚إپAsp2چ¬گ¬‹O“¹‚حپA“¯ˆê•½–ت“à‚إگ³ژOٹpŒ`‚ج’¸“_‚ةŒü‚©‚ء‚½‚و‚¤‚بŒ`‚ة‚ب‚é‚ج‚إ‚·پB‚ـ‚½پAƒذŒ‹چ‡‚ةٹض—^‚µ‚ؤ‚¢‚ب‚¢2pz‹O“¹‚ج“dژq‚حپA—×گع‚·‚é’Y‘f‚ج2pz‹O“¹‚ج‘¤–ت‚ئڈd‚ب‚èچ‡‚¢پAژں‚جگ}.4‚إژ¦‚·‚و‚¤‚بƒخŒ‹چ‡‚ًŒ`گ¬‚µ‚ـ‚·پB
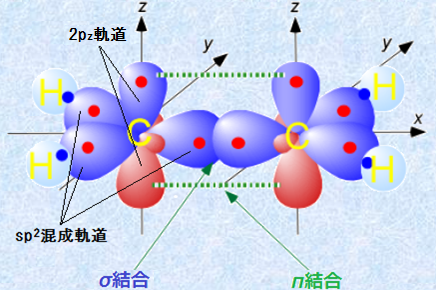
گ}.4 ƒGƒ`ƒŒƒ“C2H4‚جƒذŒ‹چ‡‚ئƒخŒ‹چ‡‚جŒ`گ¬
“ٌڈdŒ‹چ‡‚ج2–{‚جŒ‹چ‡‚ج‚¤‚؟1–{‚حپAsp2چ¬گ¬‹O“¹‚ھ2‚آ’¼گü“I‚ةڈd‚ب‚ء‚ؤگ¶‚¶‚éƒذŒ‹چ‡‚إ‚·پB2–{–ع‚جŒ‹چ‡‚جژd•û‚حپA‚±‚ê‚ئ‚حˆظ‚ب‚ء‚ؤ‚¢‚ـ‚·پB‚·‚ب‚ي‚؟پA2Œآ‚ج’Y‘f‚ج2pz‹O“¹‚ھپA‚؟‚ه‚¤‚ا•½چs‚ة‚ب‚é‚و‚¤‚ة”z’u‚³‚ê‚é‚ئپAگ}.4‚إژ¦‚·‚و‚¤‚ب2pz‹O“¹‚ج‘¤–ت‚إ‚جڈd‚ب‚è‚ھ‹N‚±‚èپAƒخŒ‹چ‡‚ئŒؤ‚خ‚ê‚錋چ‡‚ًŒ`گ¬‚·‚é‚ج‚إ‚·پB‚آ‚ـ‚èپAژہچغ‚ج’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚حپA2–{‚ج“™‰؟‚بŒ‹چ‡‚©‚ç‚إ‚«‚ؤ‚¢‚é‚ج‚إ‚ح‚ب‚پA1–{‚جƒذŒ‹چ‡‚ئ1–{‚جƒخŒ‹چ‡‚ة‚و‚éپA•تپX‚بگ«ژ؟‚ًژ‚آ2–{‚جŒ‹چ‡‚©‚çچ\گ¬‚³‚ê‚ؤ‚¢‚é‚ج‚إ‚·پBƒخŒ‹چ‡‚حپAƒذŒ‹چ‡‚ئ”ن‚ׂؤ‹O“¹“¯ژm‚جڈd‚ب‚èچ‡‚¢‚ھژم‚پAˆê”ت“I‚ةچ‚ƒGƒlƒ‹ƒMپ[‚إپA•sˆہ’è‚بŒ‹چ‡‚إ‚·پB‚»‚ج‚½‚كپA‚و‚èژم‚چ‚ƒGƒlƒ‹ƒMپ[‚جƒخŒ‹چ‡‚حپA‚و‚è‹‚’لƒGƒlƒ‹ƒMپ[‚جƒذŒ‹چ‡‚و‚è‚àپA‚¸‚ء‚ئ‰»ٹw”½‰گ«‚ة•x‚ٌ‚إ‚¢‚ـ‚·پBƒAƒ‹ƒPƒ“‚ج”½‰‚إ‚حپA‚و‚èژم‚¢ƒخŒ‹چ‡‚ھپA”½‰‚جڈê‚ة‚ب‚é‚ج‚إ‚·پB
‚»‚µ‚ؤپA‚±‚ج‹O“¹ƒ‚ƒfƒ‹‚ً—p‚¢‚é‚ئپA•\.1‚ةڈq‚ׂ½“ٌڈdŒ‹چ‡‚ج“ء’¥‚ھگà–¾‚إ‚«‚ـ‚·پB‚·‚ب‚ي‚؟پA“ٌڈdŒ‹چ‡‚جژ²‚ـ‚ي‚è‚ج‰ٌ“]‚ھ‘jٹQ‚³‚ê‚ؤ‚¢‚é‚ج‚حپA‰ٌ“]‚ھ‹N‚±‚邽‚ك‚ة‚حپAƒخŒ‹چ‡‚ًگط’f‚µ‚ب‚¯‚ê‚خ‚ب‚ç‚ب‚¢‚©‚ç‚إ‚·پBƒGƒ`ƒŒƒ“CH2پپCH2‚ً—ل‚ة‚ئ‚é‚ئپAƒخŒ‹چ‡‚جگط’f‚ة‚حپA–ٌ259 kJ‚جƒGƒlƒ‹ƒMپ[‚ھ•K—v‚إ‚ ‚èپA‚±‚ê‚حژ؛‰·‚إٹl“¾‚إ‚«‚éƒGƒlƒ‹ƒMپ[‚و‚èپA‚ح‚é‚©‚ة‘ه‚«‚¢’l‚إ‚·پB‚»‚êŒج‚ةپA’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚إ‚حپAŒ‹چ‡ژ²‚ـ‚ي‚è‚ج‰ٌ“]‚ھ‹N‚±‚ç‚ب‚¢‚ج‚إ‚·پB‚ـ‚½پA“ٌڈdŒ‹چ‡‚ھ’PŒ‹چ‡‚و‚è‚à’Z‚¢——R‚حپA2Œآ‚ج‹¤—L‚³‚ꂽ“dژq‘خ‚ج•û‚ھپA1Œآ‚ج“dژq‘خ‚و‚è‚àپA2Œآ‚جŒ´ژqٹj‚ً‹‚ˆّ‚«•t‚¯‚é‚©‚ç‚إ‚·پB‚»‚ج‚½‚كپAŒ‹چ‡ƒGƒlƒ‹ƒMپ[‚àپA“ٌڈdŒ‹چ‡‚ج•û‚ھ‚ح‚é‚©‚ة‘ه‚«‚پA’Y‘f-’Y‘f’PŒ‹چ‡‚إ‚ح–ٌ390 kJ/molپA’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚إ‚ح–ٌ680 kJ/mol‚إ‚·پB
(ii) ƒAƒ‹ƒPƒ“‚ج–½–¼–@
ƒAƒ‹ƒPƒ“‚ج–½–¼–@‚ةٹض‚·‚éIUPAC‚ج‹K‘¥‚حپAƒAƒ‹ƒJƒ“‚ةٹض‚·‚é‹K‘¥‚ةژ—‚ؤ‚¢‚ـ‚·‚ھپA“ٌڈdŒ‹چ‡‚ج–¼ڈج‚âˆت’u‚ًژ¦‚·‚½‚ك‚ةپA‚³‚ç‚ة‚¢‚‚آ‚©‚ج‹K‘¥‚ً’ا‰ء‚·‚é•K—v‚ھ‚ ‚è‚ـ‚·پB‚ـ‚¸پAˆê”ت“I‚ةپuƒAƒ‹ƒPƒ“(alkene)پv‚حپA‘ٹ“–‚·‚é’Y‘fگ”‚جگ”ژŒ‚جŒê”ِ‚جپuaپv‚ًپueneپv‚ةٹ·‚¦‚ؤ–½–¼‚µ‚ـ‚·پB2Œآˆبڈم‚ج“ٌڈdŒ‹چ‡‚ھ‚ ‚é‚ئ‚«‚حپAŒê”ِ‚ھپuƒWƒGƒ“(diene)پv‚âپuƒgƒٹƒGƒ“(triene)پv‚ب‚ا‚ج‚و‚¤‚ة‚ب‚è‚ـ‚·پB‚»‚µ‚ؤپA“ٌڈdŒ‹چ‡‚ًŒ`گ¬‚µ‚ؤ‚¢‚é’Y‘f‚ًٹـ‚ق‚و‚¤‚ة‚µ‚ؤچإ’·‚ج’Y‘fچ½‚ً‘I‚رپA“ٌڈdŒ‹چ‡‚ةچإ‚à‹ك‚¢––’[‚©‚ç”شچ†‚ً•t‚¯پA‚»‚ج“ٌڈdŒ‹چ‡‚ج’Y‘fŒ´ژq‚ھچإڈ¬‚ج”شچ†‚ًژ‚آ‚و‚¤‚ة‚µ‚ؤپA–½–¼‚µ‚ـ‚·پB
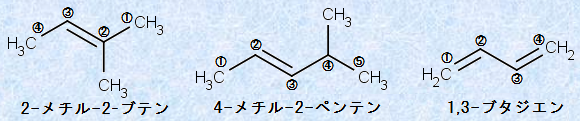
گ}.5 ƒAƒ‹ƒPƒ“‚ة‚¨‚¯‚éICPACƒVƒXƒeƒ€‚ج“K—p—ل
‚ب‚¨پA“ٌڈdŒ‹چ‡‚ھ—¼’[––‚©‚ç“™‹——£‚ة‚ ‚é‚ئ‚«‚حپAچإڈ‰‚جژ}•ھ‚©‚ê‚ةچإ‚à‹ك‚¢––’[‚©‚ç”شچ†‚ً•t‚¯‚ـ‚·(گ}.5‚ج2-ƒپƒ`ƒ‹-2-ƒuƒeƒ“‚ًژQڈئ)پB‚³‚ç‚ةپAIUPAC‚ج‹K‘¥ˆبٹO‚ة‚àپAگ”ژي‚جٹµ—p–¼‚ً’m‚ء‚ؤ‚¨‚•K—v‚ھ‚ ‚è‚ـ‚·پB—ل‚¦‚خپAٹب’P‚بƒAƒ‹ƒPƒ“‚إ‚ ‚éC2H4‚âC3H6‚حپAˆê”ت“I‚ةٹµ—p–¼‚إپAپuƒGƒ`ƒŒƒ“پv‚¨‚و‚رپuƒvƒچƒsƒŒƒ“پv‚ئŒؤ‚خ‚ê‚ؤ‚¢‚ـ‚·پB
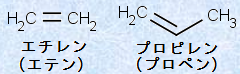
گ}.6 ٹب’P‚بƒAƒ‹ƒPƒ“‚جٹµ—p–¼
‚ـ‚½پA’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚ًٹـ‚ق2ژي‚جڈd—v‚ب’uٹ·ٹî‚ةپA‚و‚’m‚ç‚ꂽٹµ—p–¼‚ھ‚ ‚è‚ـ‚·پB‚»‚ê‚ç‚حپAپuƒrƒjƒ‹ٹî(-CHپپCH2)پv‚ئپuƒAƒٹƒ‹ٹî(-CH2-CHپپCH2)پv‚إ‚·پBژں‚جگ}.7‚ةپAپuƒrƒjƒ‹ٹîپv‚ئپuƒAƒٹƒ‹ٹîپv‚جچ\‘¢ژ®‚ًژ¦‚µ‚ـ‚·پB‚±‚ê‚ç‚ج’uٹ·ٹî–¼‚حپAژيپX‚ج‰»چ‡•¨‚جٹµ—p–¼‚ئ‚µ‚ؤ‚àژg‚ي‚ê‚ؤ‚¢‚ـ‚·پB
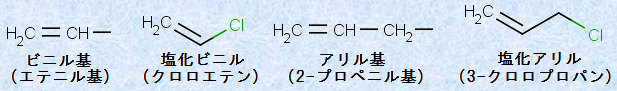
گ}.7 ƒrƒjƒ‹ٹî‚ئƒAƒٹƒ‹ٹî
(iii) ƒAƒ‹ƒPƒ“‚جٹô‰½ˆظگ«
پ@’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚إ‚حپA“ٌڈdŒ‹چ‡‚جژ²‚ـ‚ي‚è‚ج‰ٌ“]‚ھ‘©”›‚³‚ê‚ؤ‚¢‚ـ‚·پB‚»‚ج‚½‚كپA’Y‘fŒ´ژqگ”n‚ھ4ˆبڈم‚جƒAƒ‹ƒPƒ“‚إ‚حپAپuٹô‰½ˆظگ«‘ج(geometrical isomer)پv‚ئŒؤ‚خ‚ê‚é—§‘جˆظگ«‘ج‚ھ‘¶چف‚µ‚ـ‚·پB—ل‚¦‚خپA1,2-ƒWƒNƒچƒچƒGƒeƒ“‚ة‚حپAژں‚جگ}.8‚إژ¦‚·‚و‚¤‚ب2ژي‚جˆظ‚ب‚éŒ`‚ھ‚ ‚è‚ـ‚·پB

گ}.8 1,2-ƒWƒNƒچƒچƒGƒeƒ“‚جٹô‰½ˆظگ«‘ج
‚±‚ê‚ç‚جƒNƒچƒچٹî(-Cl)‚حپA‚»‚ꂼ‚êپucis(ƒ‰ƒeƒ“Œê‚إ“¯‚¶‘¤)پv‚âپutrans(ƒ‰ƒeƒ“Œê‚إ”½‘خ‘¤)پv‚ئŒؤ‚خ‚ê‚éٹضŒW‚ة‚ ‚è‚ـ‚·پBٹô‰½ˆظگ«‘ج‚حپAŒ´ژq‚â’uٹ·ٹî‚ج‹َٹش“I‚ب”z’u‚ھŒف‚¢‚ةˆظ‚ب‚邾‚¯‚إ‚·پB‚µ‚©‚µپA‚»‚ꂾ‚¯‚إپAˆظگ«‘ج‚ج•¨—“I‚¨‚و‚ر‰»ٹw“I‚بگ«ژ؟‚حپAŒف‚¢‚ةˆظ‚ب‚ء‚½‚à‚ج‚ة‚ب‚è‚ـ‚·پB
‚ـ‚½پAٹô‰½ˆظگ«‘ج‚حپA‚»‚ꂼ‚ê‚ھ“ئ—§‚µ‚½‰»چ‡•¨‚إ‚·پBڈي‰·‚إ‚حپA“ٌڈdŒ‹چ‡‚ـ‚ي‚è‚ج‰ٌ“]‚ة‚و‚ء‚ؤپA‘ٹŒف‚ة•دٹ·‚³‚ê‚邱‚ئ‚ح‚ظ‚ئ‚ٌ‚ا‹N‚±‚è‚ـ‚¹‚ٌپB‚±‚ê‚ç‚ج1,2-ƒWƒNƒچƒچƒGƒeƒ“‚ً‘ٹŒف•دٹ·‚·‚é‚ة‚حپA‚»‚جƒخŒ‹چ‡‚جگط’f‚ةڈ\•ھ‚بƒGƒlƒ‹ƒMپ[‚ً‹ں‹‹‚µپAˆّ‚«‘±‚¢‚ؤگط‚ꂸ‚ةژc‚ء‚ؤ‚¢‚éƒذŒ‹چ‡‚ج‚ـ‚ي‚è‚ة‰ٌ“]‚ً‹N‚±‚·•K—v‚ھ‚ ‚è‚ـ‚·پB‚±‚ê‚ة•K—v‚بƒGƒlƒ‹ƒMپ[‚حپAŒُ‚ـ‚½‚ح”M‚ة‚و‚ء‚ؤ‹ں‹‹‚إ‚«‚ـ‚·پB

گ}.9 ٹô‰½ˆظگ«‘ج‚ج‘ٹŒف•دٹ·
(iv) ƒAƒ‹ƒPƒ“‚ج•¨—“Iگ«ژ؟
ƒAƒ‹ƒPƒ“‚ج•¨—“Iگ«ژ؟‚حپAƒAƒ‹ƒJƒ“‚ة—قژ—‚µ‚ؤ‚¢‚ـ‚·پB‚µ‚©‚µپAƒAƒ‹ƒPƒ“‚جڈL‚¢‚حپA‚â‚âژhŒƒگ«‚ھ‹‚پA‚ق‚µ‚댙‚بڈL‚¢‚ھ‚µ‚ـ‚·پBژ–ژہ‚ئ‚µ‚ؤپAƒAƒ‹ƒPƒ“‚جŒأ‚¢ٹµ—p–¼‚إ‚ ‚éپuƒIƒŒƒtƒBƒ“(olefin)پv‚حپu–û(oil)پv‚ة—R—ˆ‚µپA‚»‚جڈL‹C‚ًژv‚¢‹N‚±‚³‚¹‚é–¼‘O‚إ‚·پBژں‚ج•\.2‚ةپAژه‚بƒAƒ‹ƒJƒ“‚ئƒAƒ‹ƒPƒ“‚ج•¨—“Iگ«ژ؟‚ًژ¦‚µ‚ـ‚·پB
•\.2 ژه‚بƒAƒ‹ƒJƒ“‚ئƒAƒ‹ƒPƒ“‚ج•¨—“Iگ«ژ؟
|
–¼ڈج |
‰»ٹwژ® |
—Z“_(پژ) |
•¦“_(پژ) |
|
ƒGƒ^ƒ“ |
CH3CH3 |
-183 |
-89 |
|
ƒvƒچƒpƒ“ |
CH3CH2CH3 |
-187.6 |
-42.1 |
|
ƒuƒ^ƒ“ |
CH3CH2CH2CH3 |
-138 |
-0.5 |
|
ƒGƒ`ƒŒƒ“ |
CH2پپCH2 |
-169 |
-103.7 |
|
ƒvƒچƒsƒŒƒ“ |
CH2پپCHCH3 |
-185.2 |
-47.4 |
|
1-ƒuƒeƒ“ |
CH2پپCHCH2CH3 |
-185 |
-6.3 |
(2) ƒAƒ‹ƒPƒ“‚ج”½‰
“ٌڈdŒ‹چ‡‚ًچ\گ¬‚µ‚ؤ‚¢‚éƒخŒ‹چ‡‚حپAƒذŒ‹چ‡‚و‚è‚à•sˆہ’è‚إپA”½‰گ«‚ھچ‚‚¢‚إ‚·پB‚»‚ج‚½‚كپAƒAƒ‹ƒPƒ“‚حپAژيپX‚ج”½‰چـ‚جچUŒ‚‚ًژَ‚¯‚â‚·‚‚ب‚ء‚ؤ‚¢‚ـ‚·پBƒAƒ‹ƒPƒ“‚إ‹N‚±‚éˆê”ت“I‚ب”½‰‚حپAپu•t‰ء”½‰(addition reaction)پv‚إ‚ ‚èپAژں‚جگ}.10‚ج‚و‚¤‚ب”½‰‚ھ‹N‚±‚è‚ـ‚·پB
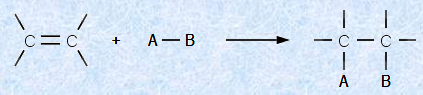
گ}.10 ƒAƒ‹ƒPƒ“‚ج•t‰ء”½‰
ƒAƒ‹ƒPƒ“‚ج•t‰ء”½‰‚إ‚حپA‚ـ‚¸ƒAƒ‹ƒPƒ“‚ج•sˆہ’è‚بƒخŒ‹چ‡‚ھٹJ—ô‚µپA”½‰چـA-B‚جƒذŒ‹چ‡‚àٹJ—ô‚µ‚ـ‚·پB‚»‚جŒ‹‰تپAƒAƒ‹ƒPƒ“‚ئ”½‰چـ‚ئ‚جٹش‚ة2ژي‚جگV‚µ‚¢ƒذŒ‹چ‡‚ھگ¶گ¬‚³‚ê‚ـ‚·پBŒ¾‚¢ٹ·‚¦‚ê‚خپA•t‰ء”½‰‚إ‚حپA1–{‚جƒخŒ‹چ‡‚ئ1–{‚جƒذŒ‹چ‡‚ھگط’f‚³‚êپA2–{‚جƒذŒ‹چ‡‚ھچى‚ç‚ê‚邱‚ئ‚ة‚ب‚è‚ـ‚·پBˆê”ت“I‚ةƒذŒ‹چ‡‚حپAƒخŒ‹چ‡‚و‚è‚à‹‚¢Œ‹چ‡‚إ‚·پB‚»‚ج‚½‚كپAƒخŒ‹چ‡‚ھƒذŒ‹چ‡‚ة•دٹ·‚³‚ê‚é•t‰ء”½‰‚حپA”½‰‘S‘ج‚ئ‚µ‚ؤ‚ح””M“I‚إپA—L—ک‚ب”½‰‚ب‚ج‚إ‚·پB
(i) ƒnƒچƒQƒ“‚ج•t‰ء(ƒnƒچƒQƒ“‰»)
‰–‘fCl2‚âڈL‘fBr2‚حپAگG”}‚ب‚µ‚إƒAƒ‹ƒPƒ“‚ة•t‰ء‚µپAپuƒrƒVƒiƒ‹“ٌƒnƒچƒQƒ“‰»•¨پv‚ً—^‚¦‚ـ‚·پBپuƒrƒVƒiƒ‹(vicinal)پv‚ئ‚حپA2‚آ‚ج—×گع‚µ‚½’Y‘fŒ´ژq‚ةŒ‹چ‡‚µ‚½پA2‚آ‚جٹ¯”\ٹî‚ًˆس–،‚µ‚ـ‚·پB‚±‚±‚إ‚حپAƒAƒ‹ƒJƒ“‚ج—×گع‚·‚é(1,2-)ˆت’u‚ةپA2‚آ‚جƒnƒچƒQƒ“‚ھ’uٹ·‚µ‚ؤ‚¢‚邱‚ئ‚ً•\‚µ‚ـ‚·پB—ل‚ئ‚µ‚ؤپAژں‚جگ}.11‚ةپAƒAƒ‹ƒPƒ“‚ة‘خ‚·‚éƒnƒچƒQƒ“‚ج•t‰ء”½‰‚ًژ¦‚µ‚ـ‚·پB
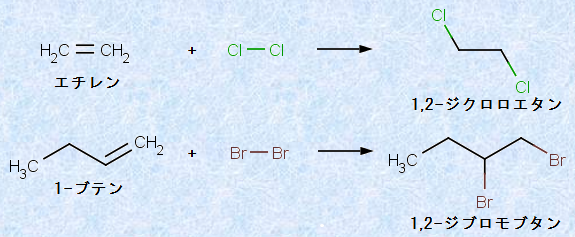
گ}.11 ƒAƒ‹ƒPƒ“‚ة‘خ‚·‚éƒnƒچƒQƒ“‚ج•t‰ء”½‰
ڈL‘fBr2‚ج•t‰ء”½‰‚حپAگشٹŒگF‰t‘ج‚ج’EگF‚ً”؛‚¤‚ج‚إپA—L‹@‰»چ‡•¨’†‚ج•s–OکaŒ‹چ‡(CپپC‚âCپكC)‚ًŒںڈo‚·‚邽‚ك‚ج‰»ٹw“IژژŒ±‚ئ‚µ‚ؤ‚و‚—p‚¢‚ç‚ê‚ـ‚·پBƒAƒ‹ƒPƒ“‚ة‘خ‚·‚éƒnƒچƒQƒ“‚ج•t‰ء”½‰‚ًچs‚¤چغ‚ة‚حپAˆê”ت“I‚ةƒnƒچƒQƒ“‚ًژl‰–‰»’Y‘fCCl4‚ب‚ا‚ج•sٹˆگ«—n”}‚ة—n‰ً‚µپA‚»‚ج—n‰t‚ًڈ‚µ‚¸‚آƒAƒ‹ƒPƒ“‚ة“H‰؛‚µ‚ؤ‚¢‚«‚ـ‚·پB‚±‚ج•t‰ء”½‰‚حپAژ؛‰·‚إ‚àڈuژ‚ة‹N‚±‚è‚ـ‚·پBڈL‘fBr2‚جژl‰–‰»’Y‘fCCl4—n‰t‚حپAگشٹŒگF‚ً’و‚µ‚ؤ‚¢‚ـ‚·‚ھپAƒAƒ‹ƒPƒ“‚ئ‚ج”½‰گ¶گ¬•¨‚حپAˆê”ت“I‚ة–³گF‚إ‚·پB‚آ‚ـ‚èپAڈL‘fBr2—n‰t‚ً‚ ‚镨ژ؟‚ة‰ء‚¦‚½‚ئ‚«‚ةپAڈL‘fBr2—n‰t‚جگشٹŒگF‚ھڈءژ¸‚·‚ê‚خپAپu‚»‚ج•¨ژ؟‚ة‚ح•s–OکaŒ‹چ‡‚ھٹـ‚ـ‚ê‚ؤ‚¢‚éپv‚ئگ„‘ھ‚إ‚«‚é‚ج‚إ‚·پB‚à‚µŒں‘ج‚ھپAƒAƒ‹ƒJƒ“‚ب‚ا‚ج–Oکa‰»چ‡•¨‚إ‚ ‚ê‚خپAڈL‘fBr2‚ئ‚ح‚±‚جڈًŒڈ‚إ‚ح”½‰‚µ‚ب‚¢‚ج‚إپAگF‚حڈء‚¦‚ـ‚¹‚ٌپB

گ}.12 ƒAƒ‹ƒPƒ“‚ةڈL‘fBr2‚ھ•t‰ء‚·‚é‚ئپAگشٹŒگF‚ھڈءژ¸‚·‚é
‚ب‚¨پA‘¼‚جƒnƒچƒQƒ“‚ج•t‰ء‚ة‚آ‚¢‚ؤ•â‘«‚·‚é‚ئپAƒtƒb‘fF2‚إ‚حپA”½‰گ«‚ھ”ٌڈي‚ةچ‚‚¢‚½‚ك‚ةŒƒ‚µ‚ƒAƒ‹ƒPƒ“‚ئ”½‰‚µپAƒrƒVƒiƒ‹“ٌƒnƒچƒQƒ“‰»•¨‚ھ‚ظ‚ئ‚ٌ‚ا“¾‚ç‚ê‚ـ‚¹‚ٌپBƒˆƒE‘fI2‚إ‚حپAƒAƒ‹ƒPƒ“‚ة•t‰ء‚ح‚µ‚ـ‚·‚ھپA•½چt‚ھ”½‰•¨‘¤‚ة•ذٹٌ‚ء‚ؤ‚¢‚é‚ج‚إپA‚à‚ئ‚جƒˆƒE‘fI2‚ئƒAƒ‹ƒPƒ“‚ة–ك‚ء‚ؤ‚µ‚ـ‚¢‚ـ‚·پBŒ‹‹ا‚ج‚ئ‚±‚ëپAƒAƒ‹ƒPƒ“‚ةŒّ—¦‚و‚•t‰ء‚·‚éƒnƒچƒQƒ“‚حپA‰–‘fCl2‚ئڈL‘fBr2‚ج‚ف‚ئ‚¢‚¤‚±‚ئ‚إ‚·پB
(ii) گ…‘f‚ج•t‰ء(گ…‘f‰»)
ƒAƒ‹ƒPƒ“‚ئگ…‘fH2‚ًژ؛‰·‰؛‚إچ¬‚؛‚ؤ‚àپA‰½‚à‹N‚±‚è‚ـ‚¹‚ٌپB‚µ‚©‚µپA‚±‚ê‚ç‚ً‹à‘®گG”}‚ج‘¶چف‰؛‚إچ¬چ‡‚·‚é‚ئپAگ…‘fH2‚ج•t‰ء”½‰‚ھŒّ—¦“I‚ةگiچs‚µپAƒAƒ‹ƒPƒ“‚حپA‘خ‰‚·‚éƒAƒ‹ƒJƒ“‚ة•دٹ·‚³‚ê‚ـ‚·پB‚±‚ج”½‰‚حپAپuگ…‘f‰»(hydrogenation)پv‚ئŒؤ‚خ‚ê‚ؤ‚¢‚ـ‚·پB
CH2پپCH2پ@پ{پ@H2پ@پ¨پ@CH3CH3
‹à‘®گG”}‚حپAˆê”ت“I‚ة”÷•²ڈَ‚جƒjƒbƒPƒ‹Ni‚â”’‹àPtپAƒpƒ‰ƒWƒEƒ€Pd‚ب‚ا‚ً—p‚¢‚ـ‚·پB‚±‚ê‚ç‚ج‹à‘®‚حپA•\–ت‚ةگ…‘fƒKƒX‚ً‹z’…‚µپAگ…‘f•ھژq‚ً‹à‘®•\–ت‚ةŒإ’肵‚ـ‚·پB‚·‚é‚ئپAگ…‘f•ھژq‚©‚çگ…‘fŒ´ژq‚ض‚ج‰ً—£‚ھ‹N‚±‚èپA‰ً—£‹z’…‚µ‚½Œ´ژq‚حپA”ٌڈي‚ة”½‰‚µ‚â‚·‚¢ڈَ‘ش‚ئ‚ب‚é‚ج‚إ‚·پB‚»‚µ‚ؤپA‚±‚جگ…‘fŒ´ژq‚ھƒAƒ‹ƒPƒ“‚ة•t‰ء‚·‚邱‚ئ‚ة‚و‚èپA‘خ‰‚·‚éƒAƒ‹ƒJƒ“‚ھگ¶گ¬‚µ‚ـ‚·پB‚±‚ج”½‰‚حپAٹزŒ³”½‰‚إ‚à‚ ‚é‚ج‚إپAپuگعگGٹزŒ³(catalytic reduction)پv‚ئ‚àŒؤ‚خ‚ê‚ؤ‚¢‚ـ‚·پB
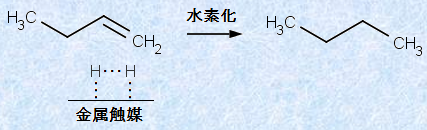
گ}.13 ƒAƒ‹ƒPƒ“‚جگ…‘f‰»
(iii) گ…‚ج•t‰ء(گ…کa”½‰)
ژ_گG”}‚ج‘¶چف‰؛‚إپAگ…‚حƒAƒ‹ƒPƒ“‚ة•t‰ء‚µ‚ـ‚·پBگ…H2O‚حپAH-OH‚جŒ‹چ‡‚إگط’f‚³‚ê‚ؤƒAƒ‹ƒPƒ“‚ة•t‰ء‚µپAگ¶گ¬•¨‚حƒAƒ‹ƒRپ[ƒ‹‚ة‚ب‚è‚ـ‚·پB—ل‚ئ‚µ‚ؤپAژں‚ةƒGƒ`ƒŒƒ“C2H4‚ئگ…H2O‚ج•t‰ء”½‰‚ًژ¦‚µ‚ـ‚·پB
CH2پپCH2پ@پ{پ@H2Oپ@پ¨پ@CH3CH2OH
‚±‚ج”½‰‚حپA’iٹK“I‚ب‹@چ\‚إگiچs‚µپA”½‰‚جˆê’iٹK–ع‚إپAژ_گG”}‚ھ•K—v‚ة‚ب‚è‚ـ‚·پB‚±‚ê‚حپA’†گ«‚بگ…•ھژq‚إ‚حپA”½‰‚ًٹJژn‚·‚邽‚ك‚جƒvƒچƒgƒ“H+ ‚ً‹ں‹‹‚إ‚«‚é‚ظ‚اپAژ_گ«“x‚ھ‹‚‚ب‚¢‚©‚ç‚إ‚·پBگ…کa”½‰‚حپAچH‹ئ“I‚ة‚à‚ئ‚«‚ة‚حژہŒ±ژ؛‚إ‚àپAƒAƒ‹ƒPƒ“‚©‚çƒAƒ‹ƒRپ[ƒ‹‚ًچ‡گ¬‚·‚é‚ج‚ة—ک—p‚³‚ê‚ؤ‚¢‚ـ‚·پBژں‚جگ}.14‚ةپAƒAƒ‹ƒPƒ“‚جگ…کa”½‰‚ًژ¦‚µ‚ـ‚·پB
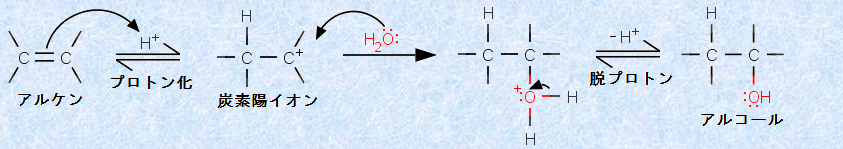
گ}.14 ƒAƒ‹ƒPƒ“‚جگ…کa”½‰
گ}.14‚ج‚و‚¤‚ةپAŒ‹چ‡‚جٹJ—ôپEŒ`گ¬—lژ®‚ً—¼گnŒ^–îˆَ‚إژ¦‚µ‚½گ}‚ًپAپu”½‰‹@چ\(reaction mechanism)پv‚ئ‚¢‚¢‚ـ‚·پB‚±‚جگ}‚ة‚¨‚¯‚é—¼گnŒ^–îˆَ‚حپA‰؟“dژq‘خ‚ج“®‚«‚ً•\‚µ‚ؤ‚¢‚ـ‚·پB—¼گnŒ^–îˆَ‚حپA“dژq‚جڈo”’n“_‚©‚çژn‚ـ‚èپAڈI’…’n“_‚إڈI‚ي‚è‚ـ‚·پB‘هٹw‚ب‚ا‚إ—L‹@‰»ٹw‚ً–{ٹi“I‚ةٹw‚شچغ‚ة‚حپA‚±‚ج–îˆَ•\‹L‚ًڈK“¾‚·‚é•K—v‚ھ‚ ‚è‚ـ‚·(—L‹@”½‰‹@چ\(‹پٹj’uٹ·”½‰‚ئ’E—£”½‰)‚ًژQڈئ)پB
(iv) ژ_‚ج•t‰ء
گ…H2O‚ج•t‰ء‚ئ“¯‚¶‚و‚¤‚ةپAٹeژي‚جژ_‚àپAƒAƒ‹ƒPƒ“‚ة•t‰ء‚µ‚ـ‚·پB‚±‚ج”½‰‚إ‚حپAƒvƒچƒgƒ“H+ ‚ھ“ٌڈdŒ‹چ‡‚جˆê•û‚ج’Y‘f‚ض•t‰ء‚µپAژ_‚جژc‚è‚ج•”•ھ‚ھپA‘¼•û‚ج’Y‘f‚ض•t‰ء‚µ‚ـ‚·پB—ل‚ئ‚µ‚ؤپAژں‚ةƒGƒ`ƒŒƒ“C2H4‚ئ‰–‰»گ…‘fHCl‚ج•t‰ء”½‰‚ًژ¦‚µ‚ـ‚·پB
CH2پپCH2 + HCl پ¨ CH3CH2Cl
‚±‚ج”½‰‚àپA’iٹK“I‚ب‹@چ\‚إگiچs‚µپA”½‰‚جˆê’iٹK–ع‚إپAƒvƒچƒgƒ“H+ ‚ئƒAƒ‹ƒPƒ“‚ھ”½‰‚µ‚ؤپA•sˆہ’è‚ب’Y‘f—zƒCƒIƒ“‚ھگ¶گ¬‚µ‚ـ‚·پB‚»‚µ‚ؤپA‘¬‚â‚©‚ةژ_‚جژc‚è‚ج•”•ھ‚ھ’Y‘f—zƒCƒIƒ“‚ة•t‰ء‚µ‚ؤپAˆہ’è‚بگ¶گ¬•¨‚ً—^‚¦‚ـ‚·پBژں‚جگ}.15‚ةپAƒAƒ‹ƒPƒ“‚ة‘خ‚·‚éژ_HA‚ج•t‰ء”½‰‚ًژ¦‚µ‚ـ‚·پB
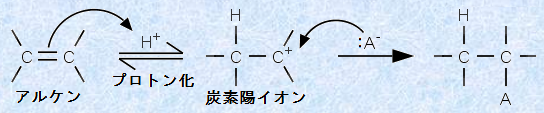
گ}.15 ƒAƒ‹ƒPƒ“‚ة‘خ‚·‚éژ_HA‚ج•t‰ء”½‰
(v) ƒIƒ]ƒ“•ھ‰ً
ƒAƒ‹ƒPƒ“‚حپAƒIƒ]ƒ“O3‚ة‘¬‚â‚©‚ةژ_‰»‚³‚ê‚ـ‚·پBƒIƒ]ƒ“O3‚حپAژ_‘fƒKƒX‚ً’ت‚¶‚ب‚ھ‚çچ‚ˆ³•ْ“d‚ًچs‚¤‚ئ”گ¶‚µپA‚»‚جƒKƒX‚ًƒAƒ‹ƒPƒ“—n‰t‚ة’ل‰·‚إ’ت‚¶‚ب‚ھ‚甽‰‚³‚¹‚ـ‚·پB‚±‚ج‚ئ‚«‚ج—n”}‚حپA‰–‰»ƒپƒ`ƒŒƒ“CH2Cl2‚ج‚و‚¤‚بˆہ’è‚ب•¨ژ؟‚ًژg‚¢‚ـ‚·پB‚±‚ج”½‰‚إ‚حپA‚ـ‚¸ƒAƒ‹ƒPƒ“‚جƒخŒ‹چ‡‚ھƒIƒ]ƒ“O3‚ئ”½‰‚µ‚ؤپAپuˆêژںƒIƒ]ƒjƒh(primary ozonide)پv‚ئŒؤ‚خ‚ê‚é3‚آ‚جژ_‘f‚ًٹـ‚ق5ˆُٹآ‚ًŒ`گ¬‚µ‚ـ‚·پB‚µ‚©‚µپAژ_‘f-ژ_‘f’PŒ‹چ‡(پ`170 kJ/mol)‚حپA”ٌڈي‚ة•sˆہ’è‚بŒ‹چ‡‚إ‚ ‚èپA‚و‚èˆہ’è‚ب’Y‘f-ژ_‘f’PŒ‹چ‡(360پ`380 kJ/mol)‚ً‘ٹ‘خ“I‚ة‘½‚—L‚·‚éپuƒIƒ]ƒjƒh(ozonide)پv‚ة‘¬‚â‚©‚ة“]ˆع‚µ‚ـ‚·پB
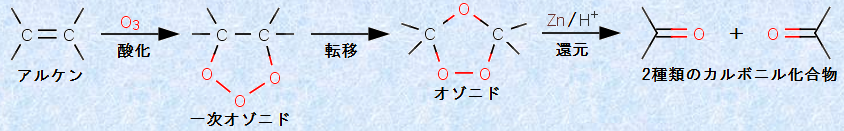
گ}.16 ƒAƒ‹ƒPƒ“‚جƒIƒ]ƒ“•ھ‰ً
‚µ‚©‚µپA‚±‚ê‚ç‚جگ¶گ¬•¨‚حپA”ڑ”گ«‚ج‚½‚ك’تڈي‚ح’P—£‚³‚ꂸپA’¼‚؟‚ةˆں‰”Zn‚ب‚ا‚جٹزŒ³چـ‚إڈˆ—‚³‚ê‚ؤپAƒJƒ‹ƒ{ƒjƒ‹‰»چ‡•¨‚ئ‚µ‚ؤ’P—£‚³‚ê‚ـ‚·پBŒ‹‹اپA‚±‚ج”½‰‚حپAƒAƒ‹ƒPƒ“‚ج“ٌڈdŒ‹چ‡‚ًٹJ—ô‚µ‚ؤپA2Œآ‚جٹe’Y‘fڈم‚ة’Y‘f-ژ_‘f“ٌڈdŒ‹چ‡(ƒJƒ‹ƒ{ƒjƒ‹ٹî)‚ًچى‚锽‰‚ب‚ج‚إ‚·پB‚±‚ج”½‰‘S‘ج‚ًپAپuƒIƒ]ƒ“•ھ‰ً(ozonolysis)پv‚ئ‚¢‚¢‚ـ‚·پBƒIƒ]ƒ“•ھ‰ً‚حپA“ٌڈdŒ‹چ‡‚جˆت’u‚ًŒˆ‚ك‚é‚ج‚ة‚و‚—ک—p‚³‚ê‚ـ‚·پB—ل‚¦‚خپA1-ƒuƒeƒ“CH2پپCHCH2CH3‚ًƒIƒ]ƒ“•ھ‰ً‚·‚é‚ئپA2ژي—ق‚جˆظ‚ب‚éƒAƒ‹ƒfƒqƒh‚ھگ¶گ¬‚µ‚ـ‚·‚ھپA2-ƒuƒeƒ“CH3CHپپCHCH3‚©‚ç‚حپA1ژي—ق‚جƒAƒ‹ƒfƒqƒh‚µ‚©گ¶گ¬‚µ‚ـ‚¹‚ٌپB
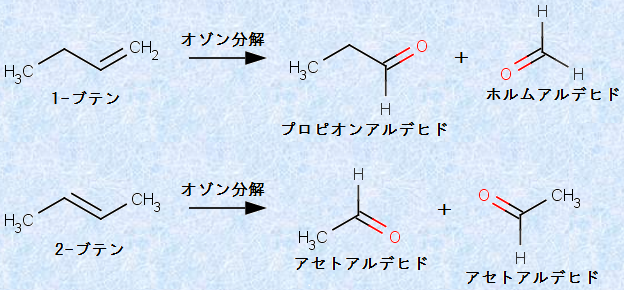
گ}.17 ƒuƒeƒ“‚جƒIƒ]ƒ“•ھ‰ً
‚±‚ج‚و‚¤‚ةپA‰½‚جƒJƒ‹ƒ{ƒjƒ‹‰»چ‡•¨‚ھگ¶گ¬‚·‚é‚ج‚©‚ً’²‚ׂ邱‚ئ‚ة‚و‚ء‚ؤپA”½‰•¨‚ھپu‚ا‚جƒuƒeƒ“ˆظگ«‘ج‚إ‚ ‚é‚©پv‚ھ—eˆص‚ة•ھ‚©‚é‚ج‚إ‚·پB‚³‚ç‚ةپAƒIƒ]ƒ“•ھ‰ً‚جگ¶گ¬•¨‚جچ\‘¢‚©‚ç‹t‚ة‚½‚ا‚邱‚ئ‚إپA–¢’m‚جƒAƒ‹ƒPƒ“‚جچ\‘¢‚ھگ„’è‚إ‚«‚ـ‚·پBƒIƒ]ƒ“•ھ‰ً‚حپA—L‹@‰»ٹw‚جچ\‘¢Œˆ’è–â‘è‚إ•pڈo‚ج”½‰‚إ‚·پB
(vi) ‰كƒ}ƒ“ƒKƒ“ژ_ƒCƒIƒ“‚ة‚و‚éژ_‰»
ƒAƒ‹ƒPƒ“‚حپA‰كƒ}ƒ“ƒKƒ“ژ_ƒCƒIƒ“MnO4- ‚ة‚àژ_‰»‚³‚ê‚ـ‚·پB‚½‚¾‚µپA‰كƒ}ƒ“ƒKƒ“ژ_ƒCƒIƒ“MnO4- ‚حپA‰tگ«‚ة‚و‚ء‚ؤژ_‰»—ح‚ھ•د‰»‚·‚é‚ج‚إپAڈًŒڈ‚ة‚و‚ء‚ؤ‚حپA“¾‚ç‚ê‚éگ¶گ¬•¨‚ھˆظ‚ب‚è‚ـ‚·پB–â‘è‚ً‰ً‚‚ئ‚«‚ة‚حپA•K‚¸–â‘蕶‚ةژwژ¦‚ھ‚ ‚é‚ح‚¸‚ب‚ج‚إپA‚و‚’چˆس‚µ‚ؤ‰؛‚³‚¢پB
‚ـ‚¸پAƒAƒ‹ƒPƒ“‚ً‰–ٹîگ«‰كƒ}ƒ“ƒKƒ“ژ_ƒJƒٹƒEƒ€KMnO4گ…—n‰t‚ئ’ل‰·‚إ”½‰‚³‚¹‚é‚ئپAƒAƒ‹ƒPƒ“‚ھƒqƒhƒچƒLƒV‰»‚³‚êپAپuƒOƒٹƒRپ[ƒ‹(glycol)پv‚ھ“¾‚ç‚ê‚ـ‚·پBƒOƒٹƒRپ[ƒ‹‚حپA—×گع‚µ‚½’Y‘f‚ة2‚آ‚جƒqƒhƒچƒLƒVٹî(-OH)‚ًژ‚آ‰»چ‡•¨‚ج‚±‚ئ‚إ‚ ‚èپA‚±‚ج”½‰‚حپAƒOƒٹƒRپ[ƒ‹‚جڈd—v‚بچ‡گ¬–@‚إ‚à‚ ‚è‚ـ‚·پB‚»‚µ‚ؤپA”½‰‚ھگi‚ق‚ة‚آ‚ê‚ؤپA‰كƒ}ƒ“ƒKƒ“ژ_ƒCƒIƒ“MnO4- ‚جگشژ‡گF‚ھڈء‚¦‚ؤپA“ٌژ_‰»ƒ}ƒ“ƒKƒ“MnO2‚جچ•ٹŒگF’¾“a‚ھگ¶‚¶‚邱‚ئ‚©‚çپA‚±‚ج”½‰‚حپAƒAƒ‹ƒPƒ“‚جŒںڈo”½‰‚ئ‚µ‚ؤ‚à—ک—p‚³‚ê‚ـ‚·پB
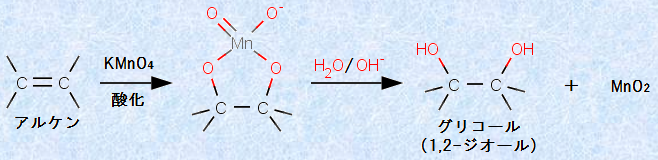
گ}.18 ƒAƒ‹ƒPƒ“‚ئ‰–ٹîگ«‰كƒ}ƒ“ƒKƒ“ژ_ƒJƒٹƒEƒ€KMnO4‚ج”½‰
ˆê•û‚إپAƒAƒ‹ƒPƒ“‚ًژ_گ«‰كƒ}ƒ“ƒKƒ“ژ_ƒJƒٹƒEƒ€KMnO4‚إ”M‚·‚é‚ئپA’†ٹشگ¶گ¬•¨‚ئ‚ب‚éƒOƒٹƒRپ[ƒ‹‚حٹJ—ô‚µپAچإڈI“I‚ة‚حپAƒPƒgƒ“‚âƒJƒ‹ƒ{ƒ“ژ_‚ة‚ـ‚إژ_‰»‚³‚ê‚ـ‚·پB‚ـ‚½پAŒ³‚جƒAƒ‹ƒPƒ“‚ج––’[‚ة“ٌڈdŒ‹چ‡‚ھ‚ ‚éڈêچ‡‚حپAگ…H2O‚ئ“ٌژ_‰»’Y‘fCO2‚ة‚ـ‚إژ_‰»‚³‚ê‚ـ‚·پB‚±‚ج”½‰‚àپAˆê”ت“I‚ة‚حƒIƒ]ƒ“•ھ‰ً‚ئ“¯—l‚ةپA“ٌڈdŒ‹چ‡‚جˆت’u‚ًŒˆ‚ك‚é‚ج‚ة—ک—p‚³‚ê‚ؤ‚¢‚ـ‚·پB
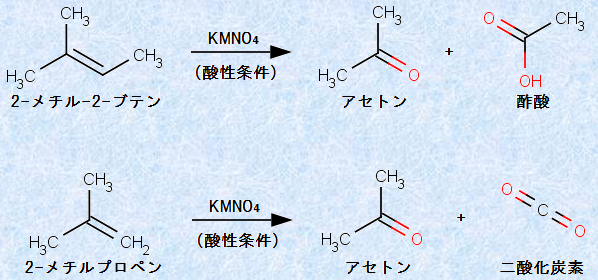
گ}.19 ƒAƒ‹ƒPƒ“‚ئژ_گ«‰كƒ}ƒ“ƒKƒ“ژ_ƒJƒٹƒEƒ€KMnO4‚ج”½‰
“ٌژ_‰»’Y‘fCO2‚ھ”گ¶‚·‚éڈêچ‡‚حپA‚»‚ج‚±‚ئ‚ھپuٹ¸‚¦‚ؤ–â‘蕶‚ةڈ‘‚©‚ê‚ؤ‚¢‚ب‚¢پv‚±‚ئ‚ھ‚ ‚è‚ـ‚·پBƒAƒ‹ƒPƒ“‚ئژ_گ«‰كƒ}ƒ“ƒKƒ“ژ_ƒJƒٹƒEƒ€KMnO4‚ةٹض‚·‚é–â‘è‚ً‰ً‚¢‚ؤ‚¢‚ؤپA’Y‘fگ”‚ھ‚ا‚¤‚µ‚ؤ‚àچ‡‚ي‚ب‚¢ڈêچ‡‚حپA“ٌژ_‰»’Y‘fCO2‚ھ”گ¶‚µ‚ؤپA’Y‘fگ”‚ھ1Œ¸ڈ‚µ‚½‚ئچl‚¦‚ؤ‚ف‚ؤ‚‚¾‚³‚¢پB‚»‚±‚ھچ\‘¢Œˆ’è‚جƒuƒŒƒCƒNƒXƒ‹پ[‚ة‚ب‚é‚©‚à‚µ‚ê‚ـ‚¹‚ٌپB
(3) ƒ}ƒ‹ƒRƒtƒjƒRƒt‘¥
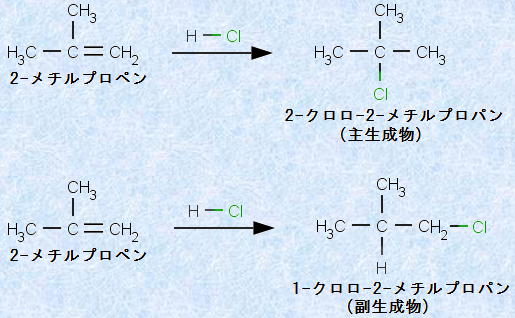
چ¶‰E”ٌ‘خڈج‚بƒAƒ‹ƒPƒ“‚ة‘خ‚µ‚ؤپAچ¶‰E”ٌ‘خڈج‚ب”½‰چـ‚ھ•t‰ء‚·‚é‚ئ‚«پAŒ´—“I‚ة‚حپA2ژي—ق‚جگ¶گ¬•¨‚ھگ¶گ¬‰آ”\‚إ‚·پB—ل‚¦‚خپA2-ƒپƒ`ƒ‹ƒvƒچƒpƒ“‚ة‰–‰»گ…‘fHCl‚ھ•t‰ء‚·‚é‚ئپA2-ƒNƒچƒچ-2-ƒپƒ`ƒ‹ƒvƒچƒpƒ“‚ئ1-ƒNƒچƒچ-2-ƒپƒ`ƒ‹ƒvƒچƒpƒ“‚ج2ژي—ق‚جگ¶گ¬•¨‚ھچl‚¦‚ç‚ê‚ـ‚·پB‚µ‚©‚µپA‚±‚ج‚¤‚؟‘Oژز‚ھژهگ¶گ¬•¨‚ئ‚ب‚èپAŒمژز‚ھ•›گ¶گ¬•¨‚ئ‚ب‚è‚ـ‚·پB
گ}.20 2-ƒپƒ`ƒ‹ƒvƒچƒpƒ“‚ئ‰–‰»گ…‘fHCl‚ج”½‰
‚±‚ج‚و‚¤‚بŒ»ڈغ‚حپAگج‚©‚ç’m‚ç‚ê‚ؤ‚¨‚èپA‚±‚جژي‚ج•t‰ء”½‰‚ًگ”‘½‚’²‚ׂ½Œ‹‰تپAƒچƒVƒA‚ج‰»ٹwژز‚إ‚ ‚éƒEƒ‰ƒWƒ~پ[ƒ‹پEƒ}ƒ‹ƒRƒtƒjƒRƒt‚حپA1870”N‚ةژں‚ج‚و‚¤‚ب–@‘¥‚ًژw“E‚µ‚ـ‚µ‚½پB‚·‚ب‚ي‚؟پAپuƒAƒ‹ƒPƒ“‚ة‘خ‚·‚éƒnƒچƒQƒ“‰»گ…‘f‚ج•t‰ء”½‰‚ة‚¨‚¢‚ؤ‚حپA‚و‚葽’uٹ·‚جƒnƒچƒQƒ“‰»•¨‚ھگ¶گ¬‚·‚éپv‚ئ‚¢‚¤‚ج‚إ‚·پB‚±‚ê‚حŒ¾‚¢ٹ·‚¦‚é‚ئپAپu‚و‚葽‚‚جگ…‘f‚ھŒ‹چ‡‚µ‚ؤ‚¢‚é’Y‘f‚ة‘خ‚µ‚ؤپA”½‰چـ‚جگ…‘f‚ھ•t‰ء‚µ‚½گ¶گ¬•¨‚ج•û‚ھژهگ¶گ¬•¨‚ة‚ب‚éپv‚ئ‚¢‚¤‚±‚ئ‚إ‚·پB‚±‚ج–@‘¥‚حپA”ق‚ج–¼‚ًژو‚ء‚ؤپAپuƒ}ƒ‹ƒRƒtƒjƒRƒt‘¥(Markovnikovپfs rule)پv‚ئŒؤ‚خ‚ê‚ؤ‚¢‚ـ‚·پB‚±‚ج–@‘¥‚حپAژہŒ±‚و‚蓱‚«ڈo‚³‚ꂽŒoŒ±‘¥‚إ‚·‚ھپAŒ»چف‚ج‰»ٹw—ک_‚إ‚حپA‚ا‚ج‚و‚¤‚ةگà–¾‚إ‚«‚é‚إ‚µ‚ه‚¤‚©پH
“ٌڈdŒ‹چ‡‚جƒخ“dژq‚حپAƒذ“dژq‚و‚è‚àٹO‘¤‚ةچL‚ھ‚ء‚ؤ‚¢‚邽‚كپA”½‰چـ‚جچUŒ‚‚ًژَ‚¯‚â‚·‚¢Œ`‚ً‚µ‚ؤ‚¢‚ـ‚·پB‚³‚ç‚ةپAƒخŒ‹چ‡‚حƒذŒ‹چ‡‚و‚è‚àژم‚¢‚½‚كپAƒAƒ‹ƒPƒ“‚إ•t‰ء”½‰‚جژه–ً‚ئ‚ب‚é‚ج‚حپA‚±‚جƒخ“dژq‚إ‚·پB“ٌڈdŒ‹چ‡‚حپA“dژq–L•x‚بŒ‹چ‡‚ب‚ج‚إپA—zƒCƒIƒ“‚ب‚ا‚ج“dژq‚ً‹پ‚ك‚锽‰چـ‚ة‘خ‚µ‚ؤپAƒخ“dژq‚ً‹ں‹‹‚·‚é–ًٹ„‚ً‰‰‚¶‚邱‚ئ‚ة‚ب‚è‚ـ‚·پB‚±‚ج‚ئ‚«‚ةپAƒAƒ‹ƒPƒ“‚ج‚و‚¤‚ة“dژq–L•x‚ب”½‰چـ‚ًپu‹پٹjچـ(nucleophile)پv‚ئ‚¢‚¢پA‹پٹjچـ‚ئ”½‰‚·‚é“dژq•s‘«‚ج”½‰چـ‚ًپu‹پ“dژqچـ(electrophile)پv‚ئ‚¢‚¢‚ـ‚·پB—L‹@‰»ٹw‚إ‚حپA‚»‚ꂼ‚ê‚ج“ھ•¶ژڑ‚ًژو‚ء‚ؤپA‹پٹjچـ‚حپuNuپvپA‹پ“dژqچـ‚حپuEپv‚ئ—ھ‚³‚ê‚邱‚ئ‚ھ‘½‚¢‚إ‚·پB
پ@ƒAƒ‹ƒPƒ“‚ة‘خ‚·‚éƒnƒچƒQƒ“‰»گ…‘f‚ج•t‰ء”½‰‚ة‚¨‚¢‚ؤ‚حپA’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚حƒخ“dژq‚ًژ‚ء‚ؤ‚¢‚é‚ج‚إپA‹پٹjچـ‚ئ‚µ‚ؤ“‚«‚ـ‚·پBˆê•û‚إپAƒvƒچƒgƒ“H+ ‚ح‹پ“dژqچـ‚إ‚ ‚èپA‚±‚ê‚ھƒخŒ‹چ‡‚ة‹ك•t‚‚ئپA2Œآ‚جƒخ“dژq‚حپAƒvƒچƒgƒ“H+ ‚ئ‚جٹش‚ةƒذŒ‹چ‡‚ًچى‚é‚ج‚ةژg‚ي‚ê‚ـ‚·پB‚±‚جƒذŒ‹چ‡‚جŒ`گ¬‚ة‚حپAƒخ“dژq‚ً2Œآ‚ئ‚àژg‚¤‚ج‚إپAژc‚è‚ج’Y‘fڈم‚ة‚حپAگ³“d‰×‚ھ”گ¶‚·‚邱‚ئ‚ة‚ب‚è‚ـ‚·پB‚آ‚ـ‚èپAپu’Y‘f—zƒCƒIƒ“(carbocation)پv‚ھگ¶گ¬‚·‚é‚ج‚إ‚·پBژں‚جگ}.21‚ةپAپu’Y‘f—zƒCƒIƒ“پv‚جگ¶گ¬”½‰‚ًژ¦‚µ‚ـ‚·پB
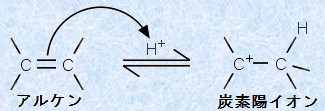
گ}.21 ’Y‘f—zƒCƒIƒ“‚جگ¶گ¬”½‰
گ¶گ¬‚µ‚½’Y‘f—zƒCƒIƒ“‚حپA‹ة‚ك‚ؤ”½‰گ«‚ھچ‚‚¢‚إ‚·پB‚»‚ج——R‚حپA—z“d‰×‚ًژ‚ء‚½’Y‘f‚ج‚ـ‚ي‚è‚ة‚حپA’تڈي‚ج’Y‘f‚ج‚و‚¤‚ة8“dژq‚إ‚ح‚ب‚پA6“dژq‚µ‚©‘¶چف‚µ‚ؤ‚¢‚ب‚¢‚©‚ç‚إ‚·پB‚±‚ج‚½‚كپA’Y‘f—zƒCƒIƒ“‚حپA2“dژq‚ً‹ں‹‹‚µ‚ؤ‚‚ê‚é‹پٹjچـ‚ئپA‘¬‚â‚©‚ةŒ‹چ‡‚µ‚ـ‚·پBˆê”ت“I‚بƒAƒ‹ƒPƒ“‚ج•t‰ء”½‰‚إ‚حپA‘وˆê’iٹK‚ج’Y‘f—zƒCƒIƒ“‚جگ¶گ¬’iٹK‚ھپA‘و“ٌ’iٹK‚ج‹پٹjچـ‚ئ‚ج”½‰‚و‚è‚àپA”½‰‘¬“x‚ھ‚¸‚ء‚ئ’x‚¢‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپA•t‰ء”½‰‘S‘ج‚ج‘¬“x‚حپA’x‚¢‘وˆê’iٹK‚ج”½‰‚ة‚و‚ء‚ؤŒˆ‚ـ‚è‚ـ‚·پB
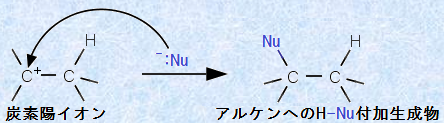
گ}.22 ’Y‘f—zƒCƒIƒ“‚ئ‹پٹjچـ‚ج”½‰
‚±‚ج‚و‚¤‚ةپAƒAƒ‹ƒPƒ“‚ج•t‰ء”½‰‚إ‚حپA’Y‘f—zƒCƒIƒ“’†ٹش‘ج‚ًŒo‚ؤپA•t‰ءگ¶گ¬•¨‚ً—^‚¦‚ؤ‚¢‚é‚ج‚إ‚·‚ھپAƒ}ƒ‹ƒRƒtƒjƒRƒt‘¥‚ةڈ]‚¦‚خپA‚و‚葽’uٹ·‚ج’Y‘f—zƒCƒIƒ“’†ٹش‘ج‚ًŒo‚ؤپA”½‰‚ھگiچs‚·‚邱‚ئ‚ة‚ب‚è‚ـ‚·پBƒAƒ‹ƒPƒ“‚ج•t‰ء”½‰‚إ‚حپA’Y‘f—zƒCƒIƒ“’†ٹش‘ج‚جگ¶گ¬’iٹK‚ھپA‘S‘ج‚ج”½‰‘¬“x‚ًŒˆ‚ك‚ؤ‚¢‚é‚ج‚إپA‚±‚ج’†ٹش‘ج‚جگ«ژ؟‚ً—‰ً‚·‚邱‚ئ‚حپA”ٌڈي‚ةڈd—v‚ب‚±‚ئ‚إ‚·پB’Y‘f—zƒCƒIƒ“‚حپAگ³“d‰×‚ًژ‚آ’Y‘fڈم‚ةپAƒAƒ‹ƒLƒ‹ٹî‚ھ‚¢‚‚آ‘¶چف‚·‚é‚©‚ة‚و‚ء‚ؤپAپu‘وژO‹‰(tertiary)پv‚ ‚é‚¢‚حپu‘و“ٌ‹‰(secondary)پvپAپu‘وˆê‹‰(primary)پv‚ة•ھ—ق‚·‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پB‘½‚‚جŒ¤‹†‚ة‚و‚ء‚ؤپA‚±‚ê‚ç‚جˆہ’èگ«‚حپAژں‚جگ}.23‚ج‚و‚¤‚ة‚ب‚邱‚ئ‚ھ•ھ‚©‚ء‚ؤ‚¢‚ـ‚·(‹@”½‰‹@چ\(‹پٹj’uٹ·”½‰‚ئ’E—£”½‰)‚ًژQڈئ)پB
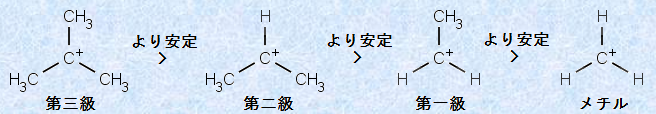
گ}.23 ’Y‘f—zƒCƒIƒ“‚جˆہ’èگ«
‚µ‚½‚ھ‚ء‚ؤپA‚و‚èˆہ’è‚ب’Y‘f—zƒCƒIƒ“’†ٹش‘ج‚ھگ¶گ¬‚·‚锽‰ŒoکH‚ظ‚اپA”½‰‘S‘ج‚ج‘¬“x‚ھ‘¬‚‚ب‚é‚ج‚إپA‹£چ‡‚µ‚½‚ئ‚«‚ةپA‚و‚è—Dگ¨‚ب”½‰‚ة‚ب‚é‚ج‚إ‚·پBƒ}ƒ‹ƒRƒtƒjƒRƒt‘¥‚ًپAŒ»‘م“I‚إ‚و‚è—L—p‚ب•\Œ»‚ةŒ¾‚¢ٹ·‚¦‚ê‚خپAپu”ٌ‘خڈج‚جƒAƒ‹ƒPƒ“‚ة”ٌ‘خڈج‚ج”½‰چـ‚ھ•t‰ء‚·‚é‚ئ‚«پAچإ‚àˆہ’è‚ب’Y‘f—zƒCƒIƒ“’†ٹش‘ج‚ھگ¶گ¬‚·‚é‚و‚¤‚ة”½‰‚ھگiچs‚·‚éپv‚ئ‚¢‚¤‚و‚¤‚ة‚ب‚è‚ـ‚·پBژہچغ‚ج‚ئ‚±‚ëپA‘وژO‹‰‚â‘و“ٌ‹‰’Y‘f—zƒCƒIƒ“‚ً’†ٹش‘ج‚ئ‚·‚锽‰‚ح‚و‚‹N‚±‚è‚ـ‚·‚ھپA‘وˆê‹‰‚ ‚é‚¢‚حƒپƒ`ƒ‹—zƒCƒIƒ“‚ً’†ٹش‘ج‚ئ‚·‚锽‰‚ح‚ظ‚ئ‚ٌ‚ا‹N‚±‚è‚ـ‚¹‚ٌپB‚±‚ج‚و‚¤‚ةپAƒAƒ‹ƒPƒ“‚ة‘خ‚·‚é•t‰ء”½‰‚حپA‹پ“dژqچـ‚ھ•t‰ء‚µ‚ؤپA’Y‘f—zƒCƒIƒ“‚ھگ¶گ¬‚·‚é’iٹK‚ھپA‘S‘ج‚ج”½‰‚ًŒˆ‚ك‚ؤ‚¢‚ـ‚·پB‚»‚ج‚½‚كپAˆê”ت“I‚ة‚±‚ج”½‰‚حپAپu‹پ“dژq•t‰ء”½‰(electrophilic addition)پv‚ئŒؤ‚خ‚ê‚ـ‚·پB
(4) ƒGƒ`ƒŒƒ“‚جچ‡گ¬‚ئ—ک—p
ƒGƒ`ƒŒƒ“C2H4‚حپAچإ‚àٹب’P‚بƒAƒ‹ƒPƒ“‚إ‚·پB‚©‚·‚©‚ةٹأ‚¢ڈL‹C‚ً—L‚·‚é–³گF‚ج‹C‘ج‚إپA—L‹@”½‰چـ‚ج’†‚إپAچH‹ئگ¶ژYٹz‚ح‘وˆêˆت‚إ‚·پBچإ‹ك‚ج“ْ–{‚ة‚¨‚¯‚éƒGƒ`ƒŒƒ“C2H4‚ج”Nٹشگ¶ژY—ت‚حپA–ٌ700–œƒgƒ“‚ة‚à‚ب‚è‚ـ‚·پBƒGƒ`ƒŒƒ“C2H4‚ح‚ا‚ج‚و‚¤‚ةگ»‘¢‚³‚êپA‰½‚ةژg—p‚³‚ê‚ؤ‚¢‚é‚ج‚إ‚µ‚ه‚¤‚©پH‚½‚¢‚ؤ‚¢‚ج’Y‰»گ…‘f‚حپAƒNƒ‰ƒbƒLƒ“ƒO‚ة‚و‚èپAƒGƒ`ƒŒƒ“C2H4‚ة‚ب‚è‚ـ‚·پBژں‚ةپAƒGƒ^ƒ“CH4‚جƒNƒ‰ƒbƒLƒ“ƒO‚ة‚و‚éƒGƒ`ƒŒƒ“C2H4‚جگ¶گ¬”½‰‚ًژ¦‚µ‚ـ‚·پB
CH3CH3پ@پ¨پ@CH2پپCH2پ@پ{پ@H2
چH‹ئ“I‚ةگ¶ژY‚³‚ê‚éƒGƒ`ƒŒƒ“C2H4‚ج‚¤‚؟پA‚©‚ب‚è‚ج—ت‚حپAƒ|ƒٹƒGƒ`ƒŒƒ“‚ة•دٹ·‚³‚ê‚ـ‚·پBŒ»چف‚إ‚حپA‹C‘ٹڈdچ‡گG”}‚جٹJ”‚ئ—¬“®‘w‹Zڈp‚جگi•à‚ة‚و‚èپA‹C‘ٹڈdچ‡–@‚ھƒ|ƒٹƒGƒ`ƒŒƒ“گ»‘¢ƒvƒچƒZƒX‚جژه–ً‚ئ‚ب‚ء‚ؤ‚¢‚ـ‚·پB‚»‚جڈdچ‡”½‰‚حپA‹گ‘ه‚بڈdچ‡ٹي’†‚إچs‚ي‚êپAگG”}1 g“–‚½‚è3,000 gˆبڈم‚جƒ|ƒٹƒGƒ`ƒŒƒ“‚ھ“¾‚ç‚ê‚ـ‚·پBگG”}—±ژq‚ح”½‰‚ج‰ك’ِ‚إپAŒ©‚½–ع‚ة‚ح•ھ‚©‚ç‚ب‚¢‚ظ‚اڈ¬‚³‚‚ب‚é‚ج‚إپA‚±‚جگG”}‚ح‚»‚ج‚ـ‚ـگ»•i’†‚ةژc‚µ‚ؤ‚¨‚‚±‚ئ‚ھ‚إ‚«پA‰ٌژû‚ج•K—v‚ھ‚ ‚è‚ـ‚¹‚ٌپBگ¶گ¬ƒ|ƒٹƒGƒ`ƒŒƒ“—±ژq‚حپA—¬“®‘w’ê•”‚©‚çکA‘±“I‚ة”²‚«ڈo‚³‚êپA’EƒKƒX“ƒ‚ًŒo‚ؤپA‰ںڈo‹@‚ة‚و‚èƒyƒŒƒbƒgڈَ‚ة‰ءچH‚³‚ê‚ؤگ»•i‚ئ‚ب‚è‚ـ‚·پB
ƒ|ƒٹƒGƒ`ƒŒƒ“‚حپAچإ‚à’Pڈƒ‚بچ\‘¢‚ًژ‚آچ‚•ھژq‰»چ‡•¨‚إ‚ ‚èپA—eٹي‚â•ï‘•ƒtƒBƒ‹ƒ€‚ً‚ح‚¶‚كپA—lپX‚ب—p“r‚ة—ک—p‚³‚ê‚ؤ‚¢‚ـ‚·پBگ¶ژY—ت‚إ‚¢‚¦‚خپA‘Sƒvƒ‰ƒXƒ`ƒbƒN‚ج–ٌ1/4‚ھƒ|ƒٹƒGƒ`ƒŒƒ“‚إ‚·پB‚»‚ج‘¼‚ة‚àپAƒGƒ`ƒŒƒ“C2H4‚ج’Y‘f-’Y‘f“ٌڈdŒ‹چ‡‚ح”½‰گ«‚ھ‚ ‚邽‚كپA—lپX‚بچH‹ئ—L‹@”½‰چـ‚جگ»‘¢‚ج‚½‚ك‚جژه—v‚بŒ´—؟‚ئ‚ب‚è‚ـ‚·پBƒGƒ^ƒmپ[ƒ‹‚âƒGƒ`ƒŒƒ“ƒOƒٹƒRپ[ƒ‹پAگ|ژ_پAگ|ژ_ƒrƒjƒ‹پA‰–‰»ƒrƒjƒ‹‚ب‚ا‚حپA‚·‚ׂؤƒGƒ`ƒŒƒ“C2H4‚©‚çگ»‘¢‚³‚ê‚ؤ‚¢‚ـ‚·پB
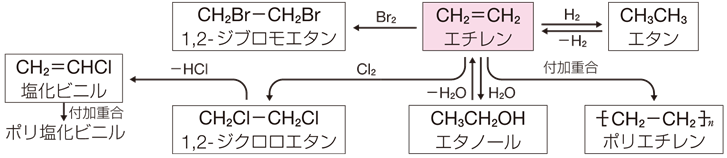
گ}.24 ƒGƒ`ƒŒƒ“C2H4‚ج”½‰
پ@ژہŒ±ژ؛‚إ‚حپAƒGƒ^ƒmپ[ƒ‹C2H5OH‚ج’Eگ…”½‰‚ة‚و‚ء‚ؤ“¾‚ـ‚·پBگG”}‚ئ‚µ‚ؤڈ—ت‚ج”Z—°ژ_H2SO4‚ھ•K—v‚إ‚ ‚èپA‰·“xŒv‚جگو’[•”‚ً‰t’†‚ةگZ‚µپA180پژ‚ً•غ‚آ‚و‚¤‚ة‰ء”M‚µ‚ـ‚·پBˆہ‘S•r‚حپAگ…‘…‚جگ…‚ھ‹t—¬‚µ‚ؤپAƒtƒ‰ƒXƒR“à‚ة“ü‚é‚ج‚ً–h‚¬‚ـ‚·پBƒGƒ`ƒŒƒ“C2H4‚حگ…‚ة—n‚¯‚ة‚‚¢‚ج‚إپAگ…ڈم’uٹ·‚إ•كڈW‚µ‚ـ‚·پB
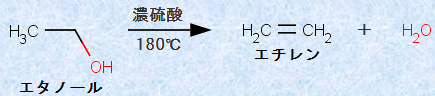
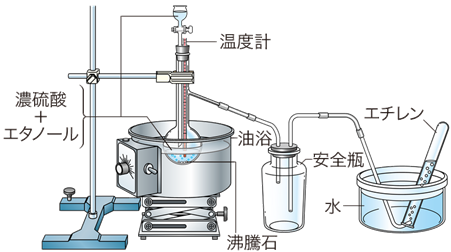
گ}.25 ƒGƒ^ƒmپ[ƒ‹C2H5OH‚ً—p‚¢‚½ƒGƒ`ƒŒƒ“C2H4‚جچ‡گ¬”½‰
(i) گA•¨ƒzƒ‹ƒ‚ƒ“‚ئ‚µ‚ؤ“‚ƒGƒ`ƒŒƒ“
ƒGƒ`ƒŒƒ“C2H4‚حپA—L‹@”½‰چـ‚جچإ‚àڈd—v‚بچH‹ئŒ´—؟‚إ‚ ‚é‚خ‚©‚è‚إ‚ب‚پA”_‹ئ‚ة‚¨‚¢‚ؤپAŒˆ’è“I‚ةڈd—v‚ب‚ ‚éژي‚جگ¶‰»ٹw“Iگ«ژ؟‚ًژ‚ء‚ؤ‚¢‚ـ‚·پB‚·‚ب‚ي‚؟پAƒGƒ`ƒŒƒ“C2H4‚حپuگA•¨ƒzƒ‹ƒ‚ƒ“پv‚إ‚ ‚èپAژيژq‚ً”‰è‚³‚¹پA‰ش‚ًٹJ‰ش‚³‚¹پA‰تژہ‚ًڈn‚µ—ژ‰ت‚³‚¹پA‚»‚µ‚ؤ—t‚â‰ش•ظ‚ً‚µ‚ع‚ـ‚¹پA‰©•د‚³‚¹‚éچى—p‚ًژ‚ء‚ؤ‚¢‚é‚ج‚إ‚·پB‚±‚ê‚حپAƒGƒ`ƒŒƒ“C2H4‚ھ—n‚¯چ‚ق‚±‚ئ‚ة‚و‚ء‚ؤپAچ×–E–Œ‚جگZ“§گ«‚ھڈم‚ھ‚èپA‚ ‚é‘مژس‰ك’ِ‚ةژhŒƒ‚ً—^‚¦‚邽‚ك‚¾‚ئچl‚¦‚ç‚ê‚ؤ‚¢‚ـ‚·پBƒGƒ`ƒŒƒ“C2H4‚ح‰تژہ‚جŒؤ‹zچى—p‚ً‘£گi‚µپAŒؤ‹z‚ًˆظڈي‘‘ه‚³‚¹‚ؤپAˆê‹C‚ة‰تژہ‚ًگ¬ڈn‚³‚¹‚ؤ‚µ‚ـ‚¤Œّ‰ت‚ھ‚ ‚é‚ج‚إ‚·پB

گ}.26 ƒŒƒ‚ƒ“‚âƒIƒŒƒ“ƒW‚حپAƒGƒ`ƒŒƒ“C2H4‚جچى—p‚ة‚و‚ء‚ؤڈnگ¬‚ً‘پ‚ك‚é
پ@20گ¢‹I‚جڈ‰‚كپAƒAƒپƒٹƒJ‚جƒJƒٹƒtƒHƒ‹ƒjƒAڈB‚إ‚حپAƒŒƒ‚ƒ“‚ً–¢ڈn‚ب—خگF‚ج‚¤‚؟‚ةژûٹn‚µپAگخ–ûƒXƒgپ[ƒu‚إ•غ‰·‚µ‚ب‚ھ‚çگ¬ڈn‚³‚¹‚ؤ‚¢‚ـ‚µ‚½پB‚ـ‚½پA‘ه—ت‚ةژûٹn‚µ‚½ƒIƒŒƒ“ƒW‚ً“S“¹—A‘—‚·‚é‚ئ‚«‚ة‚حپAٹ¦‚³‚إ“€‚é‚ج‚ً–h‚®‚½‚ك‚ةپA‰فژش‚ج’†‚إگخ–ûƒXƒgپ[ƒu‚ً•°‚¢‚ؤ‚¢‚ـ‚µ‚½پB‚±‚¤‚·‚é‚ئپAƒŒƒ‚ƒ“‚âƒIƒŒƒ“ƒW‚ج‰ت”ç‚جگF•t‚«‚ھ‚ئ‚ؤ‚à—ا‚‚ب‚邱‚ئ‚ةپA“–ژ‚ج‹ئژز‚جگl‚½‚؟‚حŒoŒ±“I‚ة‹C‚ھ•t‚¢‚ؤ‚¢‚½‚ج‚إ‚·پB‚µ‚©‚µپA”ق‚ç‚حپA‚±‚ê‚ھ•غ‰·‚ج‚½‚ك‚¾‚낤‚ئ‚خ‚©‚èچl‚¦‚ؤ‚¢‚ـ‚µ‚½پB‚»‚±‚إپAگف”ُ‚ً‹ك‘م‰»‚µپAگخ–ûƒXƒgپ[ƒu‚ًƒXƒ`پ[ƒ€ƒqپ[ƒ^پ[‚â“d‹Cƒqپ[ƒ^پ[‚ة‘م‚¦‚ؤ‚ف‚ـ‚µ‚½پB‚·‚é‚ئپAƒŒƒ‚ƒ“‚âƒIƒŒƒ“ƒW‚جگF•t‚«‚ح‚©‚¦‚ء‚ؤˆ«‚‚ب‚èپA‘ه‚«‚ب‘¹ٹQ‚ًژَ‚¯‚ـ‚µ‚½پBژہ‚حپAƒŒƒ‚ƒ“‚âƒIƒŒƒ“ƒW‚جگF•t‚«‚ھ—ا‚‚ب‚ء‚ؤ‚¢‚½‚ج‚حپA‚·‚ׂؤ‚ھگخ–ûƒXƒgپ[ƒu‚ج•sٹ®‘S”RڈؤƒKƒX‚ةٹـ‚ـ‚ê‚éƒGƒ`ƒŒƒ“C2H4‚جژd‹ئ‚¾‚ء‚½‚ج‚إ‚·پB‚»‚êˆبچ~پAƒGƒ`ƒŒƒ“C2H4‚ج‰—p‚حپAژہ—p“I‚ب‹Zڈp‚ج1‚آ‚ئ‚µ‚ؤ—ک—p‚³‚ê‚é‚و‚¤‚ة‚ب‚è‚ـ‚µ‚½پB
ƒŒƒ‚ƒ“‚âƒIƒŒƒ“ƒW‚¾‚¯‚إ‚ب‚پAƒoƒiƒi‚âƒپƒچƒ“پAƒٹƒ“ƒSپAƒJƒLپAƒ‚ƒ‚پAƒiƒVپAƒLƒEƒCƒtƒ‹پ[ƒc‚ب‚اپA‘½‚‚ج‰تژہ‚حپAƒGƒ`ƒŒƒ“C2H4‚ة‚و‚ء‚ؤگ¬ڈn‚µ‚ـ‚·پB—ل‚¦‚خپA–¢ڈn‚بƒoƒiƒiژü•س‚ج‹َ‹C‚ًƒ|ƒ“ƒv‚إ”²‚«پAŒ¸ˆ³ڈَ‘ش‚ة‚µ‚ؤƒGƒ`ƒŒƒ“C2H4‚ًڈœ‚¢‚ؤ‚ف‚é‚ئپAƒoƒiƒi‚ھ‰©گF‚گ¬ڈn‚·‚é‚ج‚ةپA”{ˆبڈم‚جژٹش‚ھ‚©‚©‚ء‚ؤ‚µ‚ـ‚¤‚ئ‚¢‚¢‚ـ‚·پB‹t‚ةƒoƒiƒiژ؛‚ج’†‚إگخ–ûƒXƒgپ[ƒu‚ً”R‚₵‚½‚肵‚ؤپAƒGƒ`ƒŒƒ“C2H4‚ج—ت‚ً‘‚₵‚ؤ‚â‚é‚ئپAƒoƒiƒi‚جگ¬ڈn‚ح‚¸‚ء‚ئ‘پ‚ـ‚è‚ـ‚·پB‚آ‚ـ‚èپA‰تژہ‚حپAژ©‚çچى‚èڈo‚·ƒGƒ`ƒŒƒ“C2H4‚ة‚و‚ء‚ؤگ¬ڈn‚·‚邵پA‘¼‚©‚ç—^‚¦‚ç‚ꂽƒGƒ`ƒŒƒ“C2H4‚ة‚و‚ء‚ؤ‚àگ¬ڈn‚·‚é‚ج‚إ‚·پB–¢ڈn‚بƒoƒiƒi‚âƒLƒEƒCƒtƒ‹پ[ƒc‚ب‚ا‚حپAƒGƒ`ƒŒƒ“C2H4‚ً”گ¶‚µ‚ة‚‚¢‚ج‚إپAƒGƒ`ƒŒƒ“C2H4‚ً”گ¶‚³‚¹‚â‚·‚¢ƒٹƒ“ƒS‚ب‚ا‚ئˆêڈڈ‚ةƒrƒjپ[ƒ‹‘ـ‚ة“ü‚ê‚ؤ‚¨‚‚ئپA‘پ‚ڈn‚µ‚ؤگH‚×چ ‚ة‚ب‚è‚ـ‚·پB

گ}.27 گخ–ûƒXƒgپ[ƒu‚حƒGƒ`ƒŒƒ“C2H4‚ً”گ¶‚³‚¹پA‰ت•¨‚جگ¬ڈn‚ً‘پ‚ك‚é
‚ـ‚½پAگA•¨‚ةƒXƒgƒŒƒX‚ً—^‚¦‚é‚ئپAƒGƒ`ƒŒƒ“C2H4‚ج”گ¶‚ھ‘£گi‚³‚ê‚邱‚ئ‚à•ھ‚©‚ء‚ؤ‚¢‚ـ‚·پB—ل‚¦‚خپAڈ•t‚¢‚½‚èƒJƒr‚ھگ¶‚¦‚½‚肵‚½ƒ~ƒJƒ“‚ھپA‹}‚ةٹأ‚‚ب‚ء‚½‚è‚·‚é‚ج‚حپA‚±‚جŒ»ڈغ‚جŒ»‚ê‚إ‚·پBگA•¨‚جژل‰è‚ھ‰½‚©‚جڈلٹQ•¨‚ة‚ش‚آ‚©‚ء‚½‚ئ‚«‚ة‚àپA‘½—ت‚جƒGƒ`ƒŒƒ“C2H4‚ھ•ْڈo‚³‚ê‚ؤپA‰è‚جŒs‚ح‘¾‚ˆç‚؟پA‹ءˆظ“I‚بگ¶–½—ح‚ًژ¦‚µ‚ـ‚·پB“¯—l‚جŒّ‰ت‚ً‚ث‚ç‚ء‚½—ل‚ئ‚µ‚ؤپAگج‚©‚çŒoŒ±“I‚ةچs‚ي‚ê‚ؤ‚¢‚éپu”“¥‚فپv‚ھ‚ ‚è‚ـ‚·پBڈHژT‚«‚ج”‚ھ”‰è‚µ‚½چغ‚ةپA‘«‚إ”‚ً“¥‚ف‚آ‚¯‚é‚ئپA‹‚ˆç‚آ‚±‚ئ‚ھ’m‚ç‚ê‚ؤ‚¢‚½‚ج‚إ‚·پB
‚³‚ç‚ةپAگA•¨‚ة‚و‚ء‚ؤ‚حپAƒGƒ`ƒŒƒ“C2H4‚ھ‹t‚ةگ¬’·‚ً–W‚°‚½‚è‚·‚邱‚ئ‚à‚ ‚è‚ـ‚·پBƒgƒEƒ‚ƒچƒRƒV‚ج•c‚ًژè‚إ–ˆ“ْ30•b‚¸‚آ25“ْٹش‚ن‚è“®‚©‚µ‚ؤپAƒXƒgƒŒƒX‚ً—^‚¦‚éژہŒ±‚ًچs‚ء‚½‚ئ‚±‚ëپA‚±‚ج•c‚حپA•پ’ت‚ج”¼•ھ‚®‚ç‚¢‚ة‚µ‚©گ¬’·‚µ‚ـ‚¹‚ٌ‚إ‚µ‚½پB‚ن‚è“®‚©‚·‚ج‚ًژ~‚ك‚é‚ئپA•c‚حŒ³’ت‚èگ¬’·‚µ‚ـ‚µ‚½پBƒCƒl‚⃀ƒM‚ج—cگA•¨‚àپA1“ْ‚ة2‰ٌ’ِ“xپA30•b‚ظ‚اژè‚إ‚³‚·‚葱‚¯‚é‚ئپA‚¾‚¢‚½‚¢20“ْ‚ظ‚اŒo‚آ‚¤‚؟‚ةپAگ¬’·‚ح’ک‚µ‚–W‚°‚ç‚ê‚ـ‚·پB
گج‚©‚çپA‹eچى‚è‚جگê–ه‰ئ‚حپAگ”–{‚جŒs‚جچ‚‚³‚ً‘µ‚¦‚é‚ج‚ةپAگL‚ر‚·‚¬‚½Œs‚ً–ˆ’©Œy‚‚ب‚إ‚ؤ‚â‚é‚»‚¤‚إ‚·پBƒvƒ‰ƒXƒ`ƒbƒN‚جگô‘َƒoƒTƒ~‚إپAŒy‚‚ح‚³‚ٌ‚إ‚â‚邱‚ئ‚à‚ ‚é‚ئ‚¢‚¢‚ـ‚·پBŒsڈن‚ھ‘µ‚¤‚ـ‚إپA‚±‚جگ¢کb‚ح‘±‚«‚ـ‚·پB‚±‚جچsˆ×‚ةپA‰بٹw“Iچھ‹’‚ح‚ ‚é‚ج‚إ‚µ‚ه‚¤‚©پB1977”N‚ةƒxƒCƒ‹‚ئƒ~ƒbƒ`ƒFƒ‹‚جچs‚ء‚½ژہŒ±‚ة‚و‚é‚ئپA‹e‚حŒs‚ج’¸•”‚ًژhŒƒ‚³‚ê‚é‚ئپAگL’·‚ھ—}گ§‚³‚ê‚ـ‚·پB“ء‚ةŒك‘O8ژپAŒكŒم4ژپAŒكŒم12ژ‚جژہŒ±Œ‹‰ت‚إ‚حپAŒك‘O8ژ‚جڈˆ—‚ج‚ئ‚«‚ةپAچإ‚à•qٹ´‚ب”½‰‚ًژ¦‚µ‚½‚ئ‚¢‚¢‚ـ‚·پB‚آ‚ـ‚èپA“ْ–{‚إگج‚©‚ç“`‚¦‚ç‚ꂽ‹eچى‚è‚ج”éŒچ‚حپAŒ©ژ–‚ة‰بٹw“Iچھ‹’‚ة— •t‚¯‚ç‚ê‚ؤ‚¢‚½‚±‚ئ‚ة‚ب‚è‚ـ‚·پB

گ}.28 ‹e‚ح–ٍ‘گ‚âٹدڈـ—pگA•¨‚ئ‚µ‚ؤپA•½ˆہژ‘م‚و‚èچح”|‚³‚ê‚ؤ‚¢‚½گA•¨‚إ‚ ‚é
پEژQچl•¶Œ£
1) H.ƒnپ[ƒg/L.E.ƒNƒŒپ[ƒ“/D.J.ƒnپ[ƒg ‹¤’کپuƒnپ[ƒgٹî‘b—L‹@‰»ٹwپv”|•—ٹظ(1986”N”چs)
2) ƒپپ[ƒgƒ‰ƒ“ƒhپEƒWƒ‡پ[ƒ“ƒYپuƒWƒ‡پ[ƒ“ƒY—L‹@‰»ٹw(ڈم)پv“Œ‹‰»ٹw“¯گl(2000”N”چs)
3) Peter W. Atkins’ک/گ猴ڈGڈ؛پEˆî—tڈح–َپu•ھژq‚ئگlٹشپv“Œ‹‰»ٹw“¯گl(1993”N”چs)
4) ژRچèٹ²•vپuگV‰»ٹw“ا–{-‰»‚¯‚éپA•د‚ي‚é‚ًٹw‚شپv”’“ْژذ(2005”N”چs)
5) چ‚”ِŒ«ˆê/‘ü–ى‹àˆê ‹¤’کپu—L‹@‰»ٹw‚ج”½‰‚ج‚µ‚‚فپv‰»ٹw‚ئ‹³ˆç65ٹھ12چ†(2017”N)
6) ˆة“Œڈحپuƒ|ƒٹƒGƒ`ƒŒƒ“پ\ƒKƒX‚©‚çƒvƒ‰ƒXƒ`ƒbƒN‚ًچى‚éپ\پv‰»ٹw‚ئ‹³ˆç66ٹھ5چ†(2018”N)