�E���~�m�[���̍����Ɖ��w����
�y�ڎ��z
(1) ��������
�@ ��^�����ǂ�3-�j�g���t�^���_1.0 g��8wt%�q�h���W�����n�t2.0 mL�������A����ɗn�}�Ƃ��ăg���G�`�����O���R�[��3 mL��������B
�A �����ǂ��A�X�s���[�^�[�ŋz�����Ȃ���A�����珬���ȉ��ł������Ɖ��M����B���M�ƂƂ��ɁA�W���F�������n�t�͐Ԋ��F�ɂȂ�B
�B �����ǂ��100���܂ŕ��₵�āA��20 mL��������B�͏o�������z��������A�n�}�������Ď����ǂɖ߂��B
�C �����ǂ�5wt%���_���i�g���E��15 mL�������A�ÐԐF�̗n�t�ɂ���B
�D �����ǂɈ��W�`�I���_�i�g���E��6.0 g�������Ă悭�U��B�n�t�͐Ԋ��F�ɂȂ�A���̂Ƃ����M����B
�E ���ʂ̐��Ŏ����ǂ̎���ɂ����ő̂���Ƃ��A�������Ȃ��悤�ɒ��ӂ��Ȃ���A3���قǎ����ǂ�U��Ȃ�����M����B
�F �M�������ɐ|�_2.0 mL�������A���炭���₷��B�������͏o������A�����ŗ�p���āA���a���z����悷��B
�G �����͐��Ő�A����������ƁA0.35 g�قǂ̃��~�m�[����������B
�H ���~�m�[��0.20 g���t���X�R����10wt%���_���i�g���E��10 mL�ɗn�����A�����200 mL�̐���������B
�I �ʂ̃t���X�R��3wt%�w�L�T�V�A�m�S(III)�J���E���n�t10 mL�A3wt%�ߎ_�����f�n�t10 mL�A��80 mL�������Ă悭������B
�J �Î����I�̗n�t���H�ɉ�����ƁA���~�m�[���̐������w���������邱�Ƃ��ł���B
(2) ���_
�q�h���W��H2N-NH2�́A�������j���������߁A3-�j�g���t�^���_�̃J���{�j����(-CO-)���j�U�������܂��B���̔����́A2���q�̐�H2O���E������u���j�I�A�V���u�������v�ł��B�������I���ƁA�E���E������5-�j�g���t�^���q�h���W�h�������܂��B�����āA����5-�j�g���t�^���q�h���W�h�̐��_���i�g���E�����n�t�ɁA�Ҍ��܂Ƃ��Ĉ��W�`�I���_�i�g���E��Na2S2O4�������ĉ��M���A�|�_CH3COOH�Œ��a����ƁA�j�g����(-NO2)���A�~�m��(-NH2)�ւƊҌ����ꂽ���~�m�[���邱�Ƃ��ł��܂��B
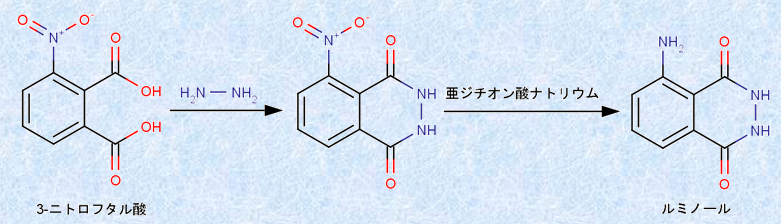
�}.1 ���~�m�[�������܂ł̔����@�\
����ꂽ���~�m�[���ɐ��_���i�g���E��NaOH�������A�S(III)�C�I��Fe3+ ��G�}�Ƃ��āA�ߎ_�����fH2O2��������ƁA�ߎ_�����ԑ̂��o�āA�t�^���_�W�A�j�I���������܂��B�ߎ_�����ԑ̂��t�^���_�W�A�j�I���ɂȂ�Ƃ��ɁA460 nm�̐������������邱�Ƃ��ł���̂ł��B���̔����������A�u���~�m�[������(luminol reaction)�v�Ƃ����܂��B
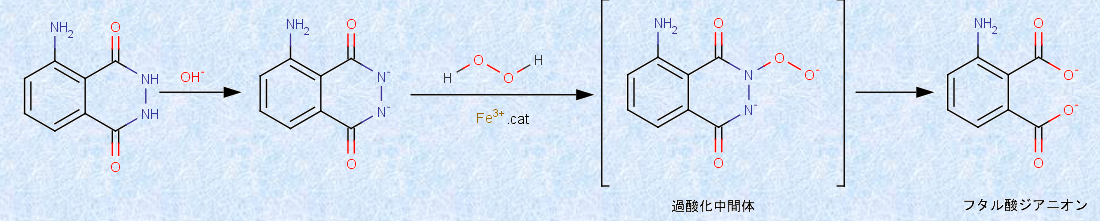
�}.2 ���w�����̔����@�\
(3) ����
�@���~�m�[���̎����́A����������3�j�g���t�^���_��4.7 mmol�A����ꂽ���~�m�[����2.0
mmol�������̂ŁA���̂悤�ɂȂ�܂��B
![]()
��肭���A���������ǂ������ɂȂ邩������܂���B�܂��A���~�m�[�������́A���t�����������̐G�}�ɂȂ�̂ŁA�x�@�̉Ȋw�{���ɂ����āA�u���t�̊ӎ��v�ɌÂ�����p�����邱�ƂŗL���ł��B�������A�h���}�Ȃǂł悭����悤�ɁA�u���~�m�[���n�t���X�v���[���āA�u���b�N���C�g�ŏƂ炷�v�Ƃ����悤�ȕ��@�����Ȃ��Ă��A�Èłŏ���Ɍ���܂��B����ɁA���~�m�[�������́A�S(III)�C�I��Fe3+ ������ΐi�s���锽���Ȃ̂ŁA�l���ȊO�ł�����܂��B�܂�A���~�m�[�������́A�u���t���ǂ����v�����ɂ߂邾���ł����āA���̌������u�^��E�V�ł��A�u�������t�ł��v�Ƃ������_���o�Ă��܂��̂ł��B���������āA���~�m�[�������́A�Ȋw�{���̒��ł��ȈՓI�ȕ��ނł���A�ٔ��̏؋��Ƃ��Ďg���邱�Ƃ́A�܂�����܂���B���~�m�[�������Łu���t�v�Ɣ���������A��ʓI�ɂ͎��Ɂu�l���ؖ������v���s���A�����Ől���ł��邱�Ƃ��������ď��߂āA�u���t�^�Ӓ�v��u��`�q�{���v�Ȃǂ̉Ȋw�{���ɉ�邱�ƂɂȂ��ł��B

�}.3 �������ɂ��������~�m�[���̉��w����