�E�������ׂĂ݂悤�I
�y�ڎ��z
(1) ��������
�@ ���f��P�̂Ɋւ��鎑�����������A���f�̏����܂Ƃ߂��J�[�h(���f�J�[�h)���쐬����B
�@�E���f�J�[�h�́A���q�ԍ�1�`20�Ԃ܂ł̌��f��Sr, Ba, Br, I, Fe, Co, Ni�̌v27��ނƂ���B
�E���f�J�[�h�ɂ��A����7��ނ̏����L�ڂ���B
�@�@�@ ���f�L���A�A ���f�̖��́A�B �����������̋�ʁA�C ���q�ʁA�D �P�̖̂��x�A�E �_�����̉��w���A�F ���f�������̉��w��
�E�_�����̉��w���́A�_�f���q���ł����������������̂������B�Ⴆ�ACO��CO2����������CO2�Ə����B
�A ���f�J�[�h�����q�ʂ̏��������ɁA������E�ֈ��ɕ��ׂ�B
�B �A�ŕ��ׂ����f�̗��K���ȏꏊ�Ő܂�Ԃ��āA�c�̗�ɍ��ځu6.�_�����̉��w���v�Ɓu7.���f�������̉��w���v�̎��Ă�����̂����Ԃ悤�ɂ���B���̂Ƃ��A���ׂ邱�Ƃ��ł��Ȃ����f�́A�e�Ɏ�菜���Ă����B

�}.1 ���f�J�[�h�̗�
(2) ���_
���f���u������(periodic
law)�v�́A���q�\�������炩�ɂȂ��ȑO���甭������Ă��܂����B���q�\�������炩�ɂȂ�܂ł̗��j�����ǂ�ƁA�܂��d�q(�g���\���A1897�N)�ƌ��q�j(���U�t�H�[�h�A1911�N)����������A�ʎq�_�Ɋ�Â����q�͌^�̒�(�{�[�A�A1913�N)������A�z�q(���U�t�H�[�h�A1917�N)�ƒ����q(�`���h�E�B�b�N�A1932�N)����������āA���q�\�������炩�ɂȂ�܂����B���q�ɂ��Ăقډ����������Ă��Ȃ���ԂŁA�������������Ӌ`�͂��Ȃ�傫���ƌ�����ł��傤�B
���f�̎������������̂́A���V�A�̉��w�҂ł���h�~�g���E�C���@�m���B�`�E�����f���[�G�t�ł��B1869�N2���A�����f���[�G�t�̓��V�A���w��ɎQ�����Ă��鑽���̉��w����1���̎����z��܂����B���̎��́u���f�̏������Ƃ��̌��q�ʂƂ̊W�v�Ƃ����_���ŁA�����f���[�G�t�́u���f�͌��q�ʂ̏��ɕ��ׂ�ƁA���w�I�����������I�Ɍ����v�Əq�ׂ܂����B�����f���[�G�t�́A���V�A��̉��w����̋��ȏ��u���w�̌����v�����M���Ă����ہA����63��ނ܂Ŕ������������Ă������f�����������@�ɔY��ł��܂����B�����f���[�G�t�́A���g���D���ȃJ�[�h�Q�[���̃\���e�B�A���甭�Ă��A���f��������������J�[�h�����x�����q�ʏ��ɕ��בւ��邱�Ƃ��J��Ԃ����ɁA1�̕\�����グ���̂ł����B�����f���[�G�t�̒�Ă����u�����\(periodic table)�v�́A�����m���Ă���63��ނ̌��f�����q�ʂ̏��������ɕ��ׁA����ɐ����̎��Ă�����̂����̗�ɕ��ׂ����̂ł���(���݂̎����\�Ƃ͏c���̎g�������t)�B
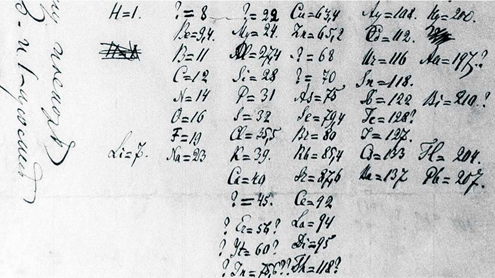
�}.2
�����f���[�G�t��1869�N2���̃��V�A���w��ŎQ���҂ɔz�z���������\�̃���
�@���̒T�������́A���ꂼ��̌��f�̐����ׂČ��f�J�[�h�����A�������ёւ��邱�ƂŁA�����f���[�G�t�����������������������̉ߒ����Č����悤�Ƃ������̂ł�(�����f���[�G�t�̎���ɂ́A�܂��M�K�X�͔�������Ă��Ȃ������̂ŁA���S�ɓ�����Ƃł͂���܂���)�B�����f���[�G�t�́A�����\�̈Ӌ`�ɂ��āA���̂悤�Ɍ���Ă��܂��B�u���f�\�͋���I�ȈӋ`�������A�܂��l�X�Ȏ��������A�W�t���邱�Ƃɂ���Ă��̌��������₷�����������łȂ��A�ގ����f�����Č��f�����ɐV�������������Ƃ����_�ŏ��R����Ȋw�������v����Ɂu���܂ʼn�X�͖��m�̌��f�̐�����\�����鉽�̎�|������������A���̌��f�̂ǂꂪ����Ȃ����A���邢�͑��݂��Ȃ����𐄒肷�邱�Ƃ��ł��Ȃ������v�ƁB
�����f���[�G�t�̎���̎����\�ɂ͂������̋�(Sc,
Ge, Ga�Ȃ�)������܂������A�����ɂ͖�����������Ă��Ȃ����f�����Ă͂܂�͂����ƁA�����f���[�G�t�͍l���܂����B�����āA�ɓ���ׂ����f�̑��݂Ƃ��̐������A�����\�ł̏㉺���E�̌��f�̐�������\�������̂ł��B�Ⴆ�A�����f���[�G�t�́A�����\�ŃA���~�j�E���̉��Ɉʒu���関�m�̌��f���u�G�J�A���~�j�E���v�A�P�C�f�̉��Ɉʒu���関�m�̌��f���u�G�J�P�C�f�v�Ɩ��t���āA�����̐�����\�����܂����B���Ȃ݂ɁA�u�G�J�v�Ƃ̓T���X�N���b�g��Łu1�v��\���܂��B�����f���[�G�t�́A�����\�ŃA���~�j�E����1���Ƃ����Ӗ��Łu�G�J�A���~�j�E���v�A�P�C�f��1���Ƃ����Ӗ��Łu�G�J�P�C�f�v�Ƃ������O�ɂ�����ł��B
���̌�A�u�G�J�A���~�j�E���v��u�G�J�P�C�f�v�����ۂɔ�������܂����B�܂�1875�N�ɂ́A�t�����X�̉��w�҂ł���|�[���E�{�A�{�[�h�������A�s���l�[�R���ō̌@���ꂽ�����̗����z���̒�����A�K���E��Ga�����܂����B���̐�������A�����f���[�G�t���u�G�J�A���~�j�E���v�Ɩ��t���Ă����A�����\�ŃA���~�j�E���̉��Ɉʒu���関�m�̌��f�ł��邱�Ƃ�������܂����B�����1886�N�ɂ́A�h�C�c�̉��w�҃N�������X�E���B���N���[���A�A���W���_�C�g�Ƃ�����z�̒�����A�Q���}�j�E��Ge�̒P���ɐ������܂����B����́A�����f���[�G�t���u�G�J�P�C�f�v�Ɩ��t���Ă����A�����\�ŃP�C�f�̉��Ɉʒu���関�m�̌��f�ł��邱�Ƃ��m�F����܂����B�����f���[�G�t���\�����������́A�������ꂽ���f�̐����Ƃ��Ȃ�߂������̂ŁA�����f���[�G�t�̖����Ǝ����\�̒n�ʂ́A�s���̂��̂ƂȂ����̂ł��B
�\.1 �@�����f���[�G�t�̗\���Ǝ��ۂ̌��f�̔�r
|
���f |
���q�� |
���q�� |
���x |
�F |
�Z�_ |
�_���� |
������ |
|
�G�J�P�C�fEs |
72 |
4 |
5.5 g/cm3 |
�D�F |
���� |
EsO2 |
EsCl4 |
|
�Q���}�j�E��Ge |
72.6 |
4 |
5.3 g/cm3 |
�D���F |
937.4 |
GeO2 |
GeCl4 |
�����f���[�G�t�����������f��\���������ƂŁA���R�̂��ƂȂ���A���������A���疽�����悤�Ƃ������w�҂����̋������n�܂�܂����B���̌�A�M�K�X���f��A�A�[�X���f�A���ː����f�̔������������A�����\�ɓ��Ă͂܂�Ȃ��Ƃ��Ĉꎞ�͋��n�ɒǂ����܂�܂������A�M�K�X���f�ɂ͐V�����g��݂��A���A�A�[�X���f����ː����f�͐��m�Ȍ��q�ʂ����肳���ɏ]���ĕ\�ɉ����āA�����\�͊�{�I�Ȍ`��ς��邱�ƂȂ����W�������܂����B�����f���[�G�t���u���E���L����]�����v�ƌĂ����\�́A���f�̕��ނ݂̂Ȃ炸�A���w�����̓W�J�Ȃǂ��܂ށA���R�̖@����F��������ɂ߂đ傫�ȓ���ƂȂ����̂ł��B
�\.2 �����f���[�G�t���\���������f�̈ꗗ
|
�����f���[�G�t�̖��� |
���ۂ̌��f�� |
�����N |
|
�G�J�A���~�j�E�� |
�K���E�� |
1875�N |
|
�G�J�{���� |
�X�J���W�E�� |
1879�N |
|
�G�J�P�C�f |
�Q���}�j�E�� |
1886�N |
|
�G�J�e���� |
�|���j�E�� |
1898�N |
|
�G�J�^���^�� |
�v���g�A�N�`�j�E�� |
1917�N |
|
*�h�r�}���K�� |
���j�E�� |
1925�N |
|
�G�J�}���K�� |
�e�N�l�`�E�� |
1937�N |
|
�G�J�Z�V�E�� |
�t�����V�E�� |
1939�N |
* �u�h�r�v�̓T���X�N���b�g��Łu2�v���Ӗ����錾�t
(3) �₢
��P�@���ׂ��\�����ۂ̎����\�Ɠ������ǂ������m�F���A�قȂ�ӏ���������̗��R���l����B
���q�ʂ̏��ɕ��ׂ�ƁAAr��K�A�����Co��Ni�̏ꏊ�ŁA���q�ԍ����Ƃ͋t�]���N����B����́A���q�ʂ����ʑ̂̕��ϒl�ŋ��߂��邽�߁A���̑��ݔ�ɂ���ĕ��ϒl�̋t�]���N���邩��ł���B
�\.3 ���q�ʂƎ�ȓ��ʑ�
|
|
18Ar |
19K |
27Co |
28Ni |
|
���q�� |
39.95 |
39.91 |
58.93 |
58.69 |
|
��ȓ��ʑ� |
36Ar�F84.2% 38Ar�F15.8% 40Ar�F0.026% |
39K�F93.2% 41K�F6.73% 40K�F0.012% |
59Co�F�ق�100% |
58Ni�F68.1% 60Ni�F26.2% 62Ni�F3.63% |
��Q�@����B�Ŏ�菜���ꂽ�J�[�h�̌��f�ɂ́A�ǂ̂悤�ȋ��ʓ_�����邩�B
�O���[�v���ł��Ȃ��̂͑J�����f(Fe, Co, Ni)�ł���A�_�������`������ۂ̌��q�̉����������傫��������A����ނ̎_���������肵�đ��݂ł����肷��A�Ȃǂ̈Ⴂ��������B�܂����f�������e�Ղɓ����Ȃ��Ȃǂ��w�E�ł���B
��R�@���ׂ����̈ȊO�ŁA���f�̎��������m�F�ł���悤�Ȍ��f�̐����ɂ́A�ǂ̂悤�Ȃ��̂����邩�B
���d�q�̐��A���q���a�A�C�I�����G�l���M�[�A�d�q�e�a�́A�d�C�A���x�Ȃǂɂ��m�F�ł���B�܂��A�P�̗̂Z�_�E���_�Ȃǂ����Ăł͂Ȃ����A������x�̎������̍����Ƃ��邱�Ƃ��ł���B
��S�@���́ia�j�`�ic�j�̃O���[�v�̌��f�̌��q�ʂɂ͂ǂ̂悤�ȊW�����邩�B19���I�̉Ȋw�҂������������[�����l���A���f�̎������ƈ�v���Ȃ����������B
�ia�j Li�CNa�CK�@�@�ib�j Be�CMg�CCa�@�@�ic�j Cl�CBr�CI
�����̃O���[�v�́A19���I�Ɂu�O�g���f���v�Ƃ��ăO���[�v�����ꂽ���̂ł���B�ގ��̐����������Ƃ͓��R�����A�����̌��q�ʂɒ��ڂ���ƁA���[��2�̕��ϒl���A�^�̌��f�̌��q�ʂɋ߂��Ȃ�̂������ł���B
�ia�j�oLi(M��6.9) �{ K(M��39�j�p�� 2 �� Na(M��23)
�ib�j�oBe(M��9.0) �{ Ca(M��40)�p�� 2 �� Mg(M��24)
�ic�j�oCl(M��35.5) �{ I(M��127�j�p�� 2 �� Br(M��80)
�����́A�قړ������ƍl����ꂽ���A��v���Ȃ��g�ݍ��킹����������ꂽ�B
ex�jMg�ECa�ESr�̏ꍇ
�@�oMg(M��24) �{ Sr�iM��88�j�p�� 2 ��
56
Ca�̌��q�ʂ�40�ň�v���Ȃ��B
��T�@���f�̎������̔����̗��j�ɂ��Ē��ׂ�B
��L�̃f�x���C�i�[�́u�O�g���f���v�ȊO�ɂ��A�j���[�����Y�́u�I�N�^�[�u���v�A�����f���[�G�t�Ɠ������ɓ��l�̎������\�\�����}�C���[�̋ƐтȂǁA�����ɂ��Ƃ܂��Ȃ��قǑ����̎��݂��������B
�E�Q�l����
1) ����́u�����f���[�G�t�Ǝ����������v���w�Ƌ���63��2��(2015�N)
2) ����O�u�����f���[�G�t�̌��f�����\�a��150�N�v���w�Ƌ���67��6��(2019�N)