・有機化合物の分離
【目次】
(1) 実験操作
① 試験管にニトロベンゼン1 mL、アニリン1 mL、安息香酸0.5 gを取り、10 mLのジエチルエーテルを加えて溶かす。
② ①の溶液を分液ろうとに入れ、1 mol/L塩酸HCl 10 mLを加えてよく振り、蒸気を逃した後、ろうと台に静置する。内容部物がはっきりと二層に分かれたら、上部から通気できるようにしてから下部のコックを開き、下層の溶液のみを試験管に取り出す。
③ ②の試験管に3 mol/L水酸化ナトリウムNaOH水溶液6 mLを加え、変化を観察する。上部に分離した物質を駒込ピペットで吸い取ってシャーレに取り、換気の良い所に放置して変化を観察する。
④ ②の分液ろうとに3 mol/L水酸化ナトリウムNaOH水溶液10 mLを加え、②と同様の操作を行った後、下層の溶液を試験管に取り出す
⑤ ④の試験管に1 mol/L塩酸HCl 5 mLを加え、変化の様子を観察する。
⑥ 分液ろうとに残ったエーテル溶液を少量シャーレに取り、換気の良い所に放置してジエチルエーテルを蒸発させ、残った物質を観察する。
(2) 理論
一般的に、多くの芳香族化合物は水に溶けにくく、ジエチルエーテルやヘキサンなどの有機溶媒には溶けやすいです。そこで、芳香族化合物の混合試料を有機溶媒に溶かし、そこへ酸や塩基の水溶液を順次加えて振り混ぜると、特定の成分だけが中和されて、塩の形になります。塩の形になった有機化合物は、有機溶媒層から水層へと転溶するので、分離が可能となります。このように、混合物から各溶媒に対する溶解性の違いを利用して、特定の成分だけを分離する操作を「抽出(extraction)」といいます。
有機化合物は、次の表.1のような酸性物質・塩基性物質・中性物質に分けられますが、このうち中性物質以外は、すべて酸塩基と中和反応が起こります。例えば、酸性物質に塩基性水溶液を加えると、中和反応が起こって水溶性の塩に変わり、有機溶媒に溶けにくくなるので、残りの物質と分離できる訳です。
表.1 有機化合物の分類
|
酸性物質 |
カルボン酸、フェノール類、スルホン酸など |
|
塩基性物質 |
アミンなど |
|
中性物質 |
アルコール、炭化水素、ニトロ化合物、エステル、アミドなど |
互いに混じり合わない2種類の液体を分離するのに、分液ろうとが用いられます。分液ろうとは、下部にコック、上部に栓の付いた球状のろうとです。今回の実験では、ニトロベンゼン・アニリン・安息香酸をジエチルエーテルに溶かし、分液ろうとを用いて分離を行っています。ジエチルエーテルの密度は0.71 g/cm3なので、ジエチルエーテルが上層、水が下層となります。

図.1 分液ろうとで有機化合物の分離を行う
ニトロベンゼン・アニリン・安息香酸を分離するには、まず実験操作②のように希塩酸HClを加えます。そして、栓の溝と本体上部の空気孔をずらし、栓の空気孔が閉じた状態になっているのを確認してから、分液ろうとを上下方向に振り動かします。振り混ぜていると、溶媒のジエチルエーテルが蒸発して、内部のガス圧が上昇してきます。そこで、頻繁にコックを開いてガスを抜き、内外圧を合わせる必要があります。これをしないと、分液ろうと内のガス圧が高まって、栓の部分から液体が激しく吹き出す危険があります。この操作を数回繰り返した後、分液ろうとをリングにかけて静置すると、上層のジエチルエーテルと下層の希塩酸HClに分離します。このとき、アニリンは希塩酸HClと反応してアニリン塩酸塩となっているので、下層の希塩酸HClに転溶しています。下層液を流出させるときは、栓の空気孔を開いた状態(栓の溝と本体上部の空気孔を合わせて、外気が通じるようにする)にして、コックを開いて下層液を取り出します。そして、二層の境界面がちょうどコックの位置に来たところでコックを閉じ、上層液と下層液を分離します。
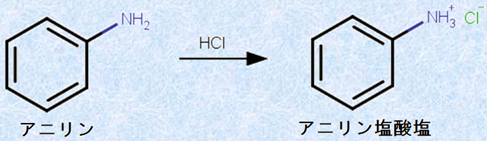
図.2 アニリンと希塩酸HClの中和反応
続いて、実験操作③のように試験管に取ったアニリン塩酸塩に水酸化ナトリウムNaOH水溶液を加えると、弱塩基の遊離が起こって、アニリンが生成します。分離したアニリンを、駒込ピペットを用いてシャーレに取ります。純粋なアニリンは無色の液体ですが、普通は淡黄色に着色しています。このアニリンを空気や光に曝しておくと、次第に酸化されて褐色になります。これは、酸化されたアニリン同士が重合を繰り返して、複雑な組成を持つ着色化合物に変化するためです。
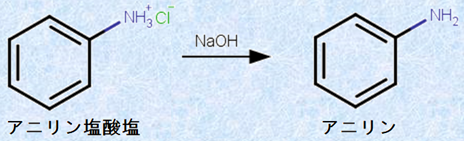
図.3 アニリン塩酸塩と水酸化ナトリウムNaOHの弱塩基遊離反応
次に、実験操作④のように分液ろうとに水酸化ナトリウムNaOH水溶液を加え、よく振り混ぜます。すると、安息香酸が水酸化ナトリウムNaOHと中和反応を起こし、安息香酸ナトリウムとなります。安息香酸ナトリウムは、下層の水酸化ナトリウムNaOH水溶液に転溶するので、分液ろうとのコックを開いて下層液だけを取り出します。
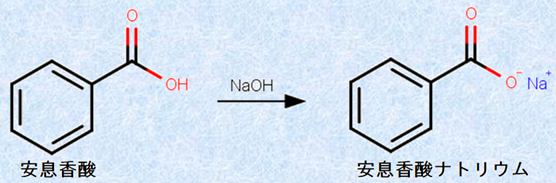
図.4 安息香酸と水酸化ナトリウムNaOHの中和反応
安息香酸ナトリウムを取り出した試験管に、操作⑤のように希塩酸HClを加えます。すると、弱酸の遊離反応が起きて、安息香酸の結晶が水溶液中に析出します。安息香酸は冷水には溶けにくいですが、熱水にはかなり溶けます。100 gの水に対する溶解度は、20℃では0.29 g、50℃では0.85 g、95℃では6.80 gです。
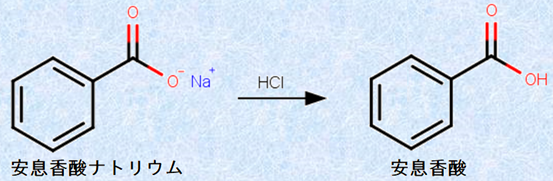
図.5 安息香酸ナトリウムと希塩酸HClの弱酸遊離反応

図.6 水溶液中に析出した安息香酸の結晶
実験操作⑥のように、最後に残ったジエチルエーテル溶液を少量摂り、換気の良い所に放置してジエチルエーテルを蒸発させると、淡黄色油状のニトロベンゼンが得られます。ニトロベンゼンは、青酸ガスHCNのようなアーモンド臭を持ち、蒸気および液体は人体に有害なので注意が必要です。

図.7 ニトロベンゼンは、水より重い(密度1.2 g/cm3)淡黄色の液体で、水に溶けにくい
・参考文献
1) 卜部吉庸「化学の新研究」三省堂(2013年発行)