پEژ_‚ئ‰–ٹî(“d—£•½چt)
(1) ژ_‰ً—£’èگ”‚≖ٹî‰ً—£’èگ”‚ئ‚ح‰½‚©پH
(6) ژمژ_پ{‹‰–ٹî‚ج‰–‚ھ‰ءگ…•ھ‰ً‚·‚éڈêچ‡(ژمژ_پ{‹‰–ٹî‚ج’†کa“_‚جpOH)
(7) ‹ژ_پ{ژم‰–ٹî‚ج‰–‚ھ‰ءگ…•ھ‰ً‚·‚éڈêچ‡(‹ژ_پ{ژم‰–ٹî‚ج’†کa“_‚جpH)
(1) ژ_‰ً—£’èگ”‚≖ٹî‰ً—£’èگ”‚ئ‚ح‰½‚©پH
پ@ƒuƒŒƒ“ƒXƒeƒbƒh‚ج’è‹`‚ة‚¨‚¯‚éژ_‚ئ‚حپAگ…‘fƒCƒIƒ“H+ ‚ً‘¼‚ج•¨ژ؟‚ة—^‚¦‚镨ژ؟‚ج‚±‚ئ‚إ‚µ‚½پB‚µ‚½‚ھ‚ء‚ؤپA“d—£“x‚ھ‘ه‚«‚¢‚ظ‚اپAژ_‚ئ‚µ‚ؤ‚ج‹‚³‚ھ‘ه‚«‚¢‚ئچl‚¦‚ç‚ê‚ـ‚·پB‚»‚±‚إپA‰½‚©1‚آ‰–ٹî‚ًŒˆ‚ك‚ؤپA‚»‚ج‰–ٹî‚ة‘خ‚·‚é“d—£“x‚ً‘ھ’è‚·‚ê‚خپAژ_‚ئ‚µ‚ؤ‚ج‹‚³‚ھ•]‰؟‚إ‚«‚ـ‚·پB’تڈيپA‚±‚جگ…‘fƒCƒIƒ“ژَ—e‘ج‚ج‰–ٹî‚ئ‚µ‚ؤ‚حپA—n”}‚ئ‚µ‚ؤ”ؤ—p‚³‚ê‚éگ…H2O‚ًچl‚¦‚ـ‚·پBژ_‚ًHA‚ئ‚µ‚ؤپAگ…H2O‚ئژ_‰–ٹ‰‚³‚¹‚é‚ئپAژں‚ج‚و‚¤‚ب‰»ٹw”½‰ژ®‚ھڈ‘‚¯‚ـ‚·پB‚±‚±‚إپAگ…‘fƒCƒIƒ“H+ ‚ً“d—£‚µ‚½‚ ‚ئ‚جA- ‚ًژ_HA‚جپu‹¤–ً‰–ٹî(conjugate base)پv‚ئ‚¢‚¢پAگ…‘fƒCƒIƒ“H+ ‚ًژَ‚¯ژو‚ء‚½ƒIƒLƒ\ƒjƒEƒ€ƒCƒIƒ“H3O+ ‚ًگ…H2O‚جپu‹¤–ًژ_(conjugate acid)پv‚ئ‚¢‚¢‚ـ‚·پB
HA(ژ_)پ@پ{پ@H2O(‰–ٹî)پ@⇄پ@A- (‹¤–ً‰–ٹî)پ@پ{پ@H3O+ (‹¤–ًژ_)
پu‹¤–ً(conjugate)پv‚ئ‚حپAˆê‘ج‚ا‚¤‚¢‚¤ˆس–،‚إ‚µ‚ه‚¤‚©پH‚±‚جژ_‰–ٹ‰‚ح‰آ‹t”½‰‚ب‚ج‚إپA‹t”½‰‚à‚ ‚é’ِ“xگiچs‚µ‚ـ‚·پB‚آ‚ـ‚èپAƒIƒLƒ\ƒjƒEƒ€ƒCƒIƒ“H3O+ ‚ھA- ‚ئژ_‰–ٹ‰‚·‚邱‚ئ‚à“–‘R‹N‚±‚肤‚邱‚ئ‚ب‚ج‚إ‚·پB‚»‚±‚إپA‹t”½‰‚ھ‹N‚±‚é‚ئ‚«‚ةژ_‚ئ‚µ‚ؤ“‚¢‚ؤ‚¢‚éƒIƒLƒ\ƒjƒEƒ€ƒCƒIƒ“H3O+ ‚ً‹¤–ًژ_پA‰–ٹî‚ئ‚µ‚ؤ“‚¢‚ؤ‚¢‚éA- ‚ً‹¤–ً‰–ٹî‚ئŒؤ‚ٌ‚إ‚¢‚é‚ج‚إ‚·پB
‚±‚جژ_‰–ٹ‰‚حپA‚ ‚é’ِ“xژٹش‚ھŒo‰ك‚·‚é‚ئپAگ³”½‰‚ئ‹t”½‰‚ج”½‰‘¬“x‚ھ“™‚µ‚‚ب‚èپA‚â‚ھ‚ؤ•½چtڈَ‘ش‚ئ‚ب‚ء‚ؤ—ژ‚؟’…‚«‚ـ‚·پB‚±‚ج‚ئ‚«‚جگ³”½‰‚ج‘¬“x‚ًv1پA‹t”½‰‚ج‘¬“x‚ًv2‚ئ‚·‚é‚ئپAژں‚ج‚و‚¤‚ة•\‚¹‚ـ‚·پB‚ب‚¨پA[H2O]‚ح—n”}‚ب‚ج‚إپAˆê”ت“I‚ة”½‰‘¬“xژ®‚ة‚حڈ‘‚«‚ـ‚¹‚ٌپB
![]()
![]()
‚»‚µ‚ؤپA•½چtڈَ‘ش‚إ‚حv1پپv2‚ھگ¬‚è—§‚ء‚ؤ‚¢‚é‚ج‚إپAKپپk1/k2‚ئ‚·‚é‚ئپAژں‚ج‚و‚¤‚ب‰»ٹw•½چt‚جژ®‚ھ“±‚«ڈo‚¹‚ـ‚·پB
![]()
![]()
‚±‚±‚إپA•½چtڈَ‘ش‚ة‚ ‚éژ_HA‚جگ…—n‰t‚ً2”{‚ة”–‚ك‚½‚ئ‰¼’肵‚ـ‚µ‚ه‚¤پBگ…—n‰t‚ً2”{‚ة”–‚ك‚é‚ج‚¾‚©‚çپA[HA], [A-], [H3O+]‚حپA‚·‚ׂؤ1/2”{‚ة‚ب‚è‚ـ‚·پB‚و‚ء‚ؤپAگ³”½‰‚ج‘¬“xv1‚ح1/2”{‚ةŒ¸ڈ‚µپA‹t”½‰‚ج‘¬“xv2‚ح1/2پ~1/2پپ1/4”{‚ةŒ¸ڈ‚·‚é‚ج‚إپAv1پ„v2‚ئ‚ب‚ء‚ؤپA‚à‚ح‚╽چtڈَ‘ش‚إ‚ح‚ب‚‚ب‚ء‚ؤ‚µ‚ـ‚¢‚ـ‚·پB‚»‚±‚إپA‚±‚ج”½‰‚ح‰E‚ضگiچs‚µپAv1‚ھŒ¸ڈ‚µ‚ؤv2‚ھ‘‰ء‚µ‚ؤ‚¢‚‚¤‚؟‚ةپA‚ ‚é‚ئ‚±‚ë‚إv1پپv2‚ئ‚ب‚ء‚ؤپAچؤ‚ر•½چtڈَ‘ش‚ة‚ب‚è‚ـ‚·پB
‚آ‚ـ‚èپAژ_‚جگ…—n‰t‚ً”–‚ك‚é‚ئپA•½چt‚ح‰E‚ةˆع“®‚µ‚ؤپA“d—£“x‚ح‘ه‚«‚‚ب‚ء‚ؤ‚¢‚‚ج‚إ‚·پB‚±‚ج‚و‚¤‚ةپA“d—£“x‚ح”Z“x‚ة‚و‚ء‚ؤ•د‚ي‚é’l‚ب‚ج‚إپAژ_‚ج‹‚³‚ً•]‰؟‚·‚éژw•W‚ئ‚µ‚ؤ‚حپAڈپX–â‘è‚ھ‚ ‚è‚ـ‚·پB‚µ‚©‚µ‚ب‚ھ‚çپAv1پپv2‚ج•½چtڈَ‘ش‚ة‚¨‚¢‚ؤپA‚ ‚鉷“xT ‚إ•½چt’èگ”K‚حڈي‚ةˆê’è‚ة•غ‚½‚ê‚é(Kپپk1/k2)‚ج‚إپA‚±‚ê‚ًKa‚ئ•\‚·‚±‚ئ‚ة‚µ‚ـ‚·پB
![]()
‚±‚جKa‚حپAژ_‚ج”Z“x‚ة‚و‚炸ˆê’è‚إ‚ ‚é‚ئ“¯ژ‚ةپA‚±‚ê‚ھ‘ه‚«‚¯‚ê‚خ•½چt‚إ‰E•س‚ج—ت‚ھ‘½‚¢‚ج‚¾‚©‚çپAژ_‚ئ‚µ‚ؤ“d—£‚ھ‚µ‚â‚·‚¢‚ئ‚¢‚¤‚±‚ئ‚à•ھ‚©‚è‚ـ‚·پB‚آ‚ـ‚èپAKa‚حژ_‚ج‹‚³‚ً•\‚·ژw•W‚ئ‚µ‚ؤژg‚¤‚±‚ئ‚ھ‚إ‚«‚é‚ج‚إ‚·پB‚±‚جKa‚ًپuژ_‰ً—£’èگ”(acid dissociation constant)پv‚ئ‚¢‚¢پA‰–ٹî‚ة‘خ‚µ‚ؤ’è‹`‚µ‚½Kb‚ًپu‰–ٹî‰ً—£’èگ”(base dissociation constant)پv‚ئ‚¢‚¢‚ـ‚·پB‚½‚¾‚µپAژ_‰ً—£’èگ”Ka‚ح”ٌڈي‚ةڈ¬‚³‚¢’l‚ة‚ب‚邱‚ئ‚ھ‘½‚¢‚ج‚إپA’تڈي‚حpH‚جڈêچ‡‚ئ“¯—l‚ةپAژ_‰ً—£’èگ”Ka‚ً•‰‚ج‘خگ”‚إ•\‚µ‚½pKa(—log10Ka)‚ھژg—p‚³‚ê‚邱‚ئ‚ھ‘½‚¢‚إ‚·پB
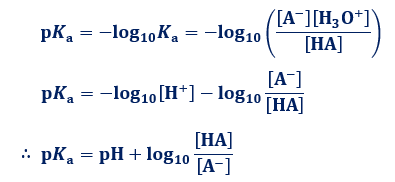
‚±‚جKa‚ب‚ç‚ر‚ةpKa‚جگ”ٹw“IٹضŒW‚ھژ¦‚·‚و‚¤‚ةپAKa‚ھ‘ه‚«‚¢‚©پA‚ ‚é‚¢‚حpKa‚ھڈ¬‚³‚¢‚ظ‚اپA‚»‚جژ_‚جژ_گ«“x‚ح‹‚‚ب‚è‚ـ‚·پBژں‚ج•\.1‚ةپA‘م•\“I‚ب‚¢‚‚آ‚©‚ج‰»چ‡•¨‚جpKa’l‚ًژ¦‚µ‚ـ‚µ‚½پBpHپپpKa‚ج‚ئ‚«‚ح1og10[HA]/[A—]پپ0‚ئ‚ب‚é‚ج‚إپA‘SHA‚ج—ت‚ج‚؟‚ه‚¤‚ا”¼•ھ‚ھ“d—£‚µ‚½ڈَ‘ش([HA]پپ[A—])‚ة‚ب‚è‚ـ‚·پB—ل‚¦‚خپAگ|ژ_CH3COOH‚حpKaپپ4.75‚ب‚ج‚إپApHپپ4.75‚ج‚ئ‚«‚ة‚ح[CH3COOH]پپ[CH3COO—]‚ئ‚ب‚è‚ـ‚·پBˆê”ت“I‚ة5ˆب‰؛‚جpKa’l‚ًژ‚آ‰»چ‡•¨‚حپAژ_گ«“x‚ھ”نٹr“I‹‚¢‚à‚ج‚إ‚ ‚é‚ئ‚ف‚ب‚³‚êپA“ء‚ة0ˆب‰؛‚جpKa’l‚ًژ‚آ‰»چ‡•¨‚حپA‹ة‚ك‚ؤژ_گ«“x‚ھ‹‚¢‚ئ‚¢‚¦‚ـ‚·پB
•\.1 ‘م•\“I‚ب‚¢‚‚آ‚©‚ج‰»چ‡•¨‚جpKa’l
|
–¼ڈج |
‰»ٹwژ® |
pKa’l |
|
‰–ژ_ |
HCl |
پ|7 |
|
—°ژ_ |
H2SO4 |
پ|3 |
|
ڈةژ_ |
HNO3 |
پ|1.3 |
|
ƒxƒ“ƒ[ƒ“ƒXƒ‹ƒzƒ“ژ_ |
C6H5SO3H |
0پ`2 |
|
گ|ژ_ |
CH3COOH |
4.75 |
|
ƒtƒFƒmپ[ƒ‹ |
C6H5OH |
10 |
|
گ… |
H2O |
15.7 |
|
ƒGƒ^ƒmپ[ƒ‹ |
C2H5OH |
15.9 |
|
ƒAƒZƒ`ƒŒƒ“ |
CHپكCH |
24 |
|
ƒAƒ“ƒ‚ƒjƒA |
NH3 |
33 |
|
ƒGƒ`ƒŒƒ“ |
CH2پپCH2 |
44 |
|
ƒپƒ^ƒ“ |
CH4 |
50 |
‚ـ‚½پAژ_‚ج‹“x‚ئ‹¤–ً‰–ٹî‚ج‹“x‚ئ‚ھپA‹t‚جٹضŒW‚ة‚ ‚é‚ئ‚¢‚¤‚±‚ئ‚ًٹo‚¦‚ؤ‚¨‚‚ئ•ض—ک‚إ‚·پB‚·‚ب‚ي‚؟پA‹¤–ً‰–ٹîA- ‚ھژم‚¢‰–ٹî‚إ‚ ‚é‚ظ‚اپA‚»‚جژ_HA‚ح‹‚¢ژ_‚ة‚ب‚è‚ـ‚·پB—ل‚¦‚خپA‰–‰»گ…‘fHCl‚ح‹‚¢ژ_‚إ‚·‚ھپA‚»‚ج‹¤–ً‰–ٹîCl- ‚حژم‚¢‰–ٹî‚إ‚·پB‚·‚ب‚ي‚؟پA‹¤–ً‰–ٹîCl- ‚حH+ ‚ة‘خ‚µ‚ؤپA”ٌڈي‚ةژم‚¢گeکaگ«‚µ‚©ژ‚ء‚ؤ‚¢‚ب‚¢‚ئ‚¢‚¤‚±‚ئ‚إ‚·پB‚»‚êŒج‚ةپA‰–‰»گ…‘fHCl‚ھ“d—£‚·‚镽چt‚ح‰E‚ةŒX‚«پA‹‚¢ژ_‚ئ‚µ‚ؤ“‚‚±‚ئ‚ة‚ب‚é‚ج‚إ‚·پB‚ـ‚½پA‚»‚ê‚ئ“¯—l‚ج——R‚إپAگ…H2O‚حژم‚¢ژ_‚إ‚ ‚é‚©‚çپA‚»‚ج‹¤–ً‰–ٹî‚جگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ح‹‚¢‰–ٹî‚إ‚·پB‹¤–ً‰–ٹîOH- ‚حH+ ‚ة‘خ‚µ‚ؤپA”ٌڈي‚ة‹‚¢گeکaگ«‚ًژ‚ء‚ؤ‚¢‚é‚ئ‚¢‚¦‚ـ‚·(ژ_‚ئ‰–ٹî(ژ_‚ئ‰–ٹî‚ج‹‚³)‚ًژQڈئ)پB
HCl(ژ_)پ@پ{پ@H2O(‰–ٹî)پ@⇄پ@Cl- (‹¤–ً‰–ٹî)پ@پ{پ@H3O+(‹¤–ًژ_)
پ@C mol/L‚ج‰–ژ_HCl‚ج[H+]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پB‰–ژ_HCl‚ح‹ژ_‚ب‚ج‚إپA“d—£“xƒ؟پà1‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپAC mol/L‚ج‰–ژ_HCl‚حپAگ…—n‰t’†‚إ‚·‚ׂؤ“d—£‚µ‚ؤ‚¢‚é‚ئچl‚¦‚ؤ–â‘è‚ ‚è‚ـ‚¹‚ٌپB‚آ‚ـ‚èپAC mol/L‚ج‰–ژ_HCl‚©‚ç‚حپAC mol/L‚جگ…‘fƒCƒIƒ“H+ ‚ھگ¶‚¶‚邱‚ئ‚ة‚ب‚è‚ـ‚·پB‚ـ‚½پA‰–ژ_HCl‚ئ“¯—l‚ةگ…H2O‚ج“d—£‚àچl‚¦‚ç‚ê‚é‚ج‚إپAگ…H2O‚©‚ç“d—£‚·‚éگ…‘fƒCƒIƒ“H+ ‚ًa mol/L‚ئ‚·‚é‚ئپAژں‚ج‚و‚¤‚ة‚ب‚è‚ـ‚·پB
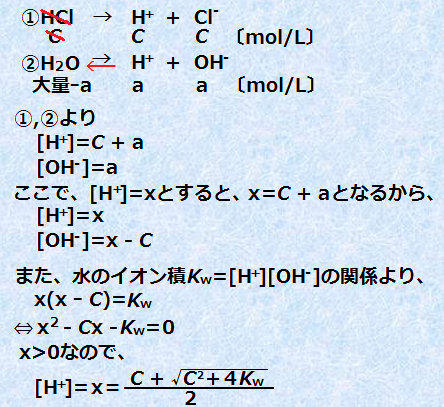
‚½‚¾‚µپAC‚ھڈ\•ھ‚ة‘ه‚«‚¢ڈًŒڈپA‚·‚ب‚ي‚؟C پ†10-6 ‚ج‚ئ‚«‚حپAژں‚ج‚و‚¤‚ةگ…H2O‚©‚ç“d—£‚·‚éگ…‘fƒCƒIƒ“H+ ‚ج—ت‚ً–³ژ‹‚µ‚ؤپAaپà0‚ئ‚µ‚ؤ‹كژ—‚·‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پB
![]()
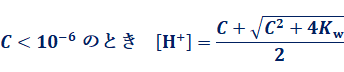
‚±‚ج‚و‚¤‚ةC پ†10-6‚إ‹كژ—‚ھ‚إ‚«‚é‚ج‚حپAگ…H2O‚ج“d—£‚ة‚و‚éa‚ھپA–³ژ‹‚إ‚«‚é‚®‚ç‚¢‚ةڈ¬‚³‚¢‚©‚ç‚إ‚·پB—ل‚¦‚خپAC پ†10-6 ‚ج‚ئ‚«‚حپACپ{aپ†10-6 ‚ھ•K‘R“I‚ةگ¬—§‚µ‚ـ‚·پB‚و‚ء‚ؤپAگ…‚جƒCƒIƒ“گدKwپپ[H+][OH-]‚جژ®‚ة[H+]پپCپ{a‚ئ[OH-]پپa‚ً‘م“ü‚·‚é‚ئپAژں‚ج‚و‚¤‚ة‚ب‚è‚ـ‚·پB
10-14پپ(Cپ{a)پ~a
Cپ{aپ†10-6 ‚ب‚ج‚إپAaپ…10-8
‚آ‚ـ‚èپAC پ†10-6 ‚ب‚ç‚خaپ…10-8 ‚ئ‚ب‚é‚ج‚إپAC‚حa‚ج100”{ˆبڈم‘ه‚«‚¢(C پ†100a)‚ئ‚¢‚¤‚±‚ئ‚ة‚ب‚è‚ـ‚·پB‚»‚µ‚ؤپA‚à‚µC ‚ئa‚إ100”{ˆبڈم‚جچ·‚ھ‚ ‚ê‚خپACپ{aپàC‚ئ‹كژ—‚µ‚ؤ‚àپAŒëچ·‚ح‚»‚ê‚ظ‚ا‘ه‚«‚‚ب‚ç‚ب‚¢‚ج‚إپAگ…H2O‚ج“d—£‚ة‚و‚éگ…‘fƒCƒIƒ“H+ ‚ج—ت‚ً–³ژ‹‚·‚邱‚ئ‚ھ‚إ‚«‚é‚ج‚إ‚·پBژہچغ‚ةC ‚ج’l‚ً•د‚¦‚ؤپAگ³ٹm‚ب[H+]‚ً‹پ‚ك‚½‚à‚ج‚ھژں‚ج•\.2‚إ‚·پB‚±‚ج•\.2‚©‚ç‚حپAC پ†10-6 ‚ب‚ç[H+]پپC‚ئ‹كژ—‚إ‚«‚é(گ…‚ج“d—£‚ً–³ژ‹‚إ‚«‚é)‚±‚ئ‚ھ•ھ‚©‚è‚ـ‚·پB
•\.2 گ…‚ج“d—£‚ًچl‚¦‚½ڈêچ‡‚جC‚ئ[H+]‚ج’l
|
Cپkmol/Lپl |
[H+]پkmol/Lپl |
|
10-3 |
1.00000001پ~10-3 |
|
10-4 |
1.000001پ~10-4 |
|
10-5 |
1.0001پ~10-5 |
|
10-6 |
1.01پ~10-6 |
|
10-7 |
1.62پ~10-7 |
|
10-8 |
1.05پ~10-7 |
|
10-9 |
1.005پ~10-7 |
‹ژ_‚ًگ…H2O‚إ1,000”{ˆبڈم‚ةٹَژك‚·‚é‚ئ‚¢‚¤‚و‚¤‚ب“ءژê‚بڈَ‹µ‚إ‚ب‚¢Œہ‚èپAC پƒ10-6 ‚جٹَ”–ژ_‚ًˆµ‚¤‚ئ‚¢‚¤‚±‚ئ‚ح‚ظ‚ئ‚ٌ‚ا‚ ‚è‚ـ‚¹‚ٌپB‚µ‚½‚ھ‚ء‚ؤپAˆê”ت“I‚ةC mol/L‚جˆê‰؟‚ج‹ژ_HA‚ج[H+]‚حپAژں‚ج‚و‚¤‚ة•\‚·‚±‚ئ‚ھ‚إ‚«‚ـ‚·پB
[H+]پپC
پ¦‚½‚¾‚µپAC پ†10-6 ‚ج‚ئ‚«‚ةŒہ‚é
پ@C mol/L‚جگ…ژ_‰»ƒiƒgƒٹƒEƒ€NaOHگ…—n‰t‚ج[OH-]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پBگ…ژ_‰»ƒiƒgƒٹƒEƒ€NaOH‚ح‹‰–ٹî‚ب‚ج‚إپA“d—£“xƒ؟پà1‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپAC mol/L‚جگ…ژ_‰»ƒiƒgƒٹƒEƒ€NaOH‚حپAگ…—n‰t’†‚إ‚·‚ׂؤ“d—£‚µ‚ؤ‚¢‚é‚ئچl‚¦‚ؤ–â‘è‚ ‚è‚ـ‚¹‚ٌپB‚آ‚ـ‚èپAC mol/L‚جگ…ژ_‰»ƒiƒgƒٹƒEƒ€NaOHگ…—n‰t‚©‚ç‚حپAC mol/L‚جگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ھگ¶‚¶‚邱‚ئ‚ة‚ب‚è‚ـ‚·پB‚ـ‚½پAگ…ژ_‰»ƒiƒgƒٹƒEƒ€NaOH‚ئ“¯—l‚ةگ…H2O‚ج“d—£‚àچl‚¦‚ç‚ê‚é‚ج‚إپAگ…H2O‚©‚ç“d—£‚·‚éگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ًa mol/L‚ئ‚·‚é‚ئپAژں‚ج‚و‚¤‚ة‚ب‚è‚ـ‚·پB

‚½‚¾‚µپAC‚ھڈ\•ھ‚ة‘ه‚«‚¢ڈًŒڈپA‚·‚ب‚ي‚؟C پ†10-6 ‚ج‚ئ‚«‚حپAژں‚ج‚و‚¤‚ةگ…H2O‚©‚ç“d—£‚·‚éگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ج—ت‚ً–³ژ‹‚µ‚ؤپAaپà0‚ئ‚µ‚ؤ‹كژ—‚·‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پB
![]()
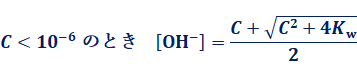
ˆê”ت“I‚ة‚حپAC پ†10-6 ‚جڈًŒڈ‚ھگ¬—§‚µ‚ؤ‚¢‚邱‚ئ‚ھ‘½‚¢‚إ‚·پB‚±‚جڈêچ‡‚حپAگ…H2O‚ج“d—£‚ة‚و‚éگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ج—ت‚ً–³ژ‹‚·‚邱‚ئ‚ھ‚إ‚«پAC mol/L‚جˆê‰؟‚ج‹‰–ٹîMOH‚ج[OH-]‚حپAژں‚ج‚و‚¤‚ة•\‚·‚±‚ئ‚ھ‚إ‚«‚ـ‚·پB
[OH-]پپC
پ¦‚½‚¾‚µپAC پ†10-6 ‚ج‚ئ‚«‚ةŒہ‚é
پ@C mol/L‚جگ|ژ_CH3COOHگ…—n‰t‚ج[H+]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پBگ|ژ_CH3COOH‚حژمژ_‚ب‚ج‚إپA“d—£“x‚حƒ؟ <<1‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپAگ…—n‰t’†‚إ‚حپAˆê•”‚جگ|ژ_CH3COOH‚¾‚¯‚ھ“d—£‚µ‚ؤ‚¢‚ـ‚·پB“d—£“x‚ًƒ؟‚ئ‚·‚é‚ئپAC mol/L‚جگ|ژ_CH3COOH‚©‚ç‚حپACƒ؟ mol/L‚جگ…‘fƒCƒIƒ“H+ ‚ھگ¶‚¶‚ـ‚·پB‚µ‚©‚µپA“d—£“xƒ؟‚ح”Z“x‚ة‚و‚ء‚ؤ‘ه‚«‚•د“®‚·‚é’l‚ب‚ج‚إپAژو‚舵‚¢‚ھ“‚¢‚إ‚·پB‚»‚±‚إپA“d—£“xƒ؟‚ًژg‚ي‚¸پA”Z“x‚ة‚و‚炸ˆê’è’l‚ًژو‚éژ_‰ً—£’èگ”Ka‚ًژg‚ء‚ؤپA[H+]‚ً‹پ‚ك‚é•û–@‚ًچl‚¦‚ؤ‚ف‚ـ‚·پB
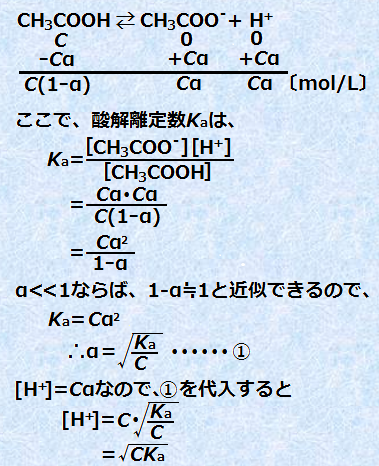
‚½‚¾‚µپA‚±‚ê‚حCƒ؟پ†10-6 ‚جڈًŒڈ‚ھگ¬—§‚µ‚ؤ‚¢‚éڈêچ‡‚ةŒہ‚è‚ـ‚·پB‚à‚µCƒ؟پƒ10-6 ‚ب‚ç‚خپAگ…H2O‚جڈo‚·گ…‘fƒCƒIƒ“H+ ‚جٹٌ—^‚ً–³ژ‹‚إ‚«‚ب‚‚ب‚ء‚ؤ‚µ‚ـ‚¤‚ج‚إپA[H+]‚ً‹پ‚ك‚éژ®‚حپAژں‚ةژ¦‚·‚و‚¤‚ب3ژں•û’ِژ®‚ج‰ً‚ة‚ب‚ء‚ؤ‚µ‚ـ‚¢‚ـ‚·پB‚±‚ê‚ًژèŒvژZ‚إ‰ً‚‚ج‚ح‘ه•دچ¢“ï‚ب‚ج‚إپA‘هٹw“üژژƒŒƒxƒ‹‚ج–â‘è‚إ‚حپA’تڈيCƒ؟ پ†10-6 ‚جڈًŒڈ‚ھ–³ڈًŒڈ‚ةگ¬—§‚µ‚ؤ‚¢‚é‚ئچl‚¦‚ؤ–â‘è‚ ‚è‚ـ‚¹‚ٌپB
![]()
‚ـ‚½1-ƒ؟پà1‚ج‹كژ—‚حپAƒ؟ <<1‚جڈêچ‡‚إ‚µ‚©—p‚¢‚邱‚ئ‚ھ‚إ‚«‚ـ‚¹‚ٌپB“d—£“xƒ؟‚ھ‚ ‚é’ِ“x‘ه‚«‚‚ب‚éڈًŒڈپA‚·‚ب‚ي‚؟ƒ؟پ„0.05(1-ƒ؟پƒ0.95)‚ج‚ئ‚«‚حپA‹كژ—‚ً—p‚¢‚¸‚ةژں‚ج2ژں•û’ِژ®‚ً‰ً‚¢‚ؤپAƒ؟‚ً‹پ‚ك‚ب‚¯‚ê‚خ‚ب‚è‚ـ‚¹‚ٌپB‚±‚ج2ژں•û’ِژ®‚ج‰ًƒ؟‚حپAƒ؟پ„0.05‚ج‚ئ‚«‚ج“d—£“x‚ئ‚ب‚è‚ـ‚·پB“d—£“xƒ؟‚ھ0.05‚و‚è‚à‘ه‚«‚¢ڈêچ‡‚إ‚حپAŒvژZ‚جŒëچ·‚ھ‘ه‚«‚‚ب‚é‚ج‚إپA1-ƒ؟پà1‚ج‹كژ—‚ھژg‚¦‚ب‚‚ب‚é‚ج‚إ‚·پB
![]()
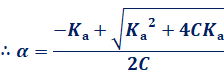
پ@‚±‚±‚إپA1-ƒ؟پà1‚ج‹كژ—‚ھژg‚¦‚ب‚¢ڈêچ‡‚ًچl‚¦‚ؤ‚ف‚ـ‚µ‚ه‚¤پB—ل‚¦‚خپAگ…—n‰t‚ًڈ\•ھ‚ة”–‚ك‚ؤپACپپKa‚ة‚ب‚ء‚½‚ئ‚«‚ج“d—£“xƒ؟‚ً‹پ‚ك‚ؤ‚ف‚ـ‚·پB‰¼‚ة1-ƒ؟پà1‚ج‹كژ—‚ھژg‚¦‚½‚ئ‚·‚é‚ئپA“d—£“xƒ؟‚ح![]() ‚ئ‚ب‚èپA‚±‚ê‚إ‚حƒ؟ <<1‚ج‰¼’è‚ة–µڈ‚‚µ‚ـ‚·پB‚»‚±‚إپAڈم‹L‚ج“ٌژں•û’ِژ®‚ةCپپKa‚ً‘م“ü‚µ‚ؤŒvژZ‚·‚é‚ئپAژں‚ج‚و‚¤‚بٹب’P‚بŒvژZ‚ئ‚ب‚è‚ـ‚·پB
‚ئ‚ب‚èپA‚±‚ê‚إ‚حƒ؟ <<1‚ج‰¼’è‚ة–µڈ‚‚µ‚ـ‚·پB‚»‚±‚إپAڈم‹L‚ج“ٌژں•û’ِژ®‚ةCپپKa‚ً‘م“ü‚µ‚ؤŒvژZ‚·‚é‚ئپAژں‚ج‚و‚¤‚بٹب’P‚بŒvژZ‚ئ‚ب‚è‚ـ‚·پB
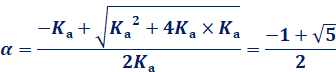
![]() ‚ئ‚µ‚ؤ“d—£“xƒ؟‚ًŒvژZ‚µ‚ؤ‚ف‚é‚ئپAƒ؟پپ0.565‚ئ‚ب‚è‚ـ‚·پB‚و‚ء‚ؤپAƒ؟پ…0.05‚ئ‚ب‚é1‚آ‚ج–عˆہ‚ھپAC>>Ka‚ئ‚¢‚¤‚±‚ئ‚ة‚à‚ب‚è‚ـ‚·پBگ|ژ_CH3COOH‚إ‚ ‚ê‚خپA25پژ‚إKaپپ2.7پ~10-5 mol/L‚ب‚ج‚إپAگ…‚إ”–‚ك‚ؤ”Z“xC‚ھ10-3 پ`10-5 mol/L‚‚ç‚¢‚ة‚ب‚é‚ئپAŒvژZ‚جŒëچ·‚ھ‘ه‚«‚‚ب‚ء‚ؤ‚«‚ـ‚·پB
‚ئ‚µ‚ؤ“d—£“xƒ؟‚ًŒvژZ‚µ‚ؤ‚ف‚é‚ئپAƒ؟پپ0.565‚ئ‚ب‚è‚ـ‚·پB‚و‚ء‚ؤپAƒ؟پ…0.05‚ئ‚ب‚é1‚آ‚ج–عˆہ‚ھپAC>>Ka‚ئ‚¢‚¤‚±‚ئ‚ة‚à‚ب‚è‚ـ‚·پBگ|ژ_CH3COOH‚إ‚ ‚ê‚خپA25پژ‚إKaپپ2.7پ~10-5 mol/L‚ب‚ج‚إپAگ…‚إ”–‚ك‚ؤ”Z“xC‚ھ10-3 پ`10-5 mol/L‚‚ç‚¢‚ة‚ب‚é‚ئپAŒvژZ‚جŒëچ·‚ھ‘ه‚«‚‚ب‚ء‚ؤ‚«‚ـ‚·پB
‚µ‚©‚µ‚ب‚ھ‚çپA“d—£“xƒ؟‚ھڈ\•ھ‚ةڈ¬‚³‚¢ڈًŒڈ(ƒ؟پ…0.05)‚ب‚çپA1-ƒ؟پà1‚ئ‹كژ—‚ھ‚إ‚«‚ـ‚·پB‚±‚جڈêچ‡‚حƒ؟پà0‚ئچl‚¦‚ؤ—ا‚¢‚ج‚إپAˆê”ت“I‚ةC mol/L‚جˆê‰؟‚جژمژ_HA‚ج[H+]‚حپAژں‚ج‚و‚¤‚ة•\‚·‚±‚ئ‚ھ‚إ‚«‚ـ‚·پB
![]()
پ¦‚½‚¾‚µپACƒ؟ پ†10-6 ‚©‚آƒ؟پ…0.05‚ج‚ئ‚«‚ةŒہ‚é
پ@C mol/L‚جƒAƒ“ƒ‚ƒjƒANH3گ…—n‰t‚ج[OH-]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پBƒAƒ“ƒ‚ƒjƒANH3‚حژم‰–ٹî‚ب‚ج‚إپA“d—£“x‚حƒ؟ <<1‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپAگ…—n‰t’†‚إ‚حپAˆê•”‚جƒAƒ“ƒ‚ƒjƒANH3‚¾‚¯‚ھ“d—£‚µ‚ؤ‚¢‚ـ‚·پB“d—£“x‚ًƒ؟‚ئ‚·‚é‚ئپAC mol/L‚جƒAƒ“ƒ‚ƒjƒANH3‚©‚ç‚حپACƒ؟ mol/L‚جگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ھگ¶‚¶‚ـ‚·پB‚µ‚©‚µپA“d—£“xƒ؟‚ح”Z“x‚ة‚و‚ء‚ؤ‘ه‚«‚•د“®‚·‚é’l‚ب‚ج‚إپAژو‚舵‚¢‚ھ“‚¢‚إ‚·پB‚»‚±‚إپA“d—£“xƒ؟‚ًژg‚ي‚¸پA”Z“x‚ة‚و‚炸ˆê’è’l‚ًژو‚鉖ٹî‰ً—£’èگ”Kb‚ًژg‚ء‚ؤپA[OH-]‚ً‹پ‚ك‚é•û–@‚ًچl‚¦‚ؤ‚ف‚ـ‚·پB
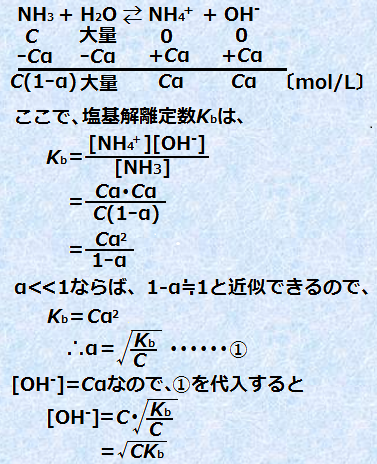
‚½‚¾‚µپA‚±‚ê‚حCƒ؟ پ†10-6 ‚جڈًŒڈ‚ھگ¬—§‚µ‚ؤ‚¢‚éڈêچ‡‚ةŒہ‚è‚ـ‚·پBCƒ؟پƒ10-6 ‚ب‚ç‚خپAگ…H2O‚جڈo‚·گ…ژ_‰»•¨ƒCƒIƒ“OH- ‚جٹٌ—^‚ً–³ژ‹‚إ‚«‚ب‚‚ب‚é‚ج‚إپA[OH-]‚ً—^‚¦‚éژ®‚ح‘ه•د•،ژG‚ة‚ب‚è‚ـ‚·پB‚±‚ê‚ًژèŒvژZ‚إ‰ً‚‚ج‚حچ¢“ï‚ب‚½‚كپAژم‰–ٹî‚جڈêچ‡‚إ‚àپACƒ؟ پ†10-6 ‚جڈًŒڈ‚ھ–³ڈًŒڈ‚ةگ¬—§‚µ‚ؤ‚¢‚é‚ئچl‚¦‚ؤ–â‘è‚ ‚è‚ـ‚¹‚ٌپB
‚ـ‚½1-ƒ؟پà1‚ج‹كژ—‚حپAƒ؟ <<1‚جڈêچ‡‚إ‚µ‚©—p‚¢‚邱‚ئ‚ھ‚إ‚«‚ـ‚¹‚ٌپB“d—£“xƒ؟‚ھ‚ ‚é’ِ“x‘ه‚«‚‚ب‚éڈًŒڈپA‚·‚ب‚ي‚؟ƒ؟پ„0.05‚ج‚ئ‚«‚حپA‹كژ—‚ً—p‚¢‚¸‚ةژں‚ج2ژں•û’ِژ®‚ً‰ً‚¢‚ؤپAƒ؟‚ً‹پ‚ك‚ب‚¯‚ê‚خ‚ب‚è‚ـ‚¹‚ٌپB
![]()
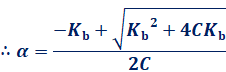
‚µ‚©‚µ‚ب‚ھ‚çپA“d—£“xƒ؟‚ھڈ\•ھ‚ةڈ¬‚³‚¢ڈًŒڈ(ƒ؟پ…0.05)‚ب‚çپA1-ƒ؟پà1‚ئ‹كژ—‚ھ‚إ‚«‚ـ‚·پB‚±‚جڈêچ‡‚حƒ؟پà0‚ئچl‚¦‚ؤ—ا‚¢‚ج‚إپAˆê”ت“I‚ةC mol/L‚جˆê‰؟‚جژم‰–ٹîMOH‚ج[OH-]‚حپAژں‚ج‚و‚¤‚ة•\‚·‚±‚ئ‚ھ‚إ‚«‚ـ‚·پB
![]()
پ¦‚½‚¾‚µپACƒ؟ پ†10-6 ‚©‚آƒ؟پ…0.05‚ج‚ئ‚«‚ةŒہ‚é
(6) ژمژ_پ{‹‰–ٹî‚ج‰–‚ھ‰ءگ…•ھ‰ً‚·‚éڈêچ‡(ژمژ_پ{‹‰–ٹî‚ج’†کa“_‚جpOH)
ژمژ_‚ئ‹‰–ٹî‚ج’†کa‚ة‚و‚ء‚ؤگ¶‚¶‚鉖‚ھگ…H2O‚ة—n‚¯‚é‚ئپAپu‰ءگ…•ھ‰ً(hydrolysis)پv‚ھ‹N‚±‚ء‚ؤژم‰–ٹîگ«‚ًژ¦‚µ‚ـ‚·پB‚±‚±‚إپAC mol/L‚جگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONaگ…—n‰t‚ج[OH-]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پBگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚حپAگ…—n‰t’†‚إ‚ح100%‚ھ“d—£‚µ‚ؤ‚¨‚èپAگ|ژ_ƒCƒIƒ“CH3COO- ‚ئƒiƒgƒٹƒEƒ€ƒCƒIƒ“Na+ ‚ئ‚ة“d—£‚µ‚ؤ‚¢‚ـ‚·پBƒiƒgƒٹƒEƒ€ƒCƒIƒ“Na+ ‚حگ…H2O‚ئ‚ح”½‰‚µ‚ـ‚¹‚ٌ‚ھپAگ|ژ_ƒCƒIƒ“CH3COO- ‚جˆê•”‚حگ…H2O‚ئ”½‰‚µ‚ـ‚·پB‚±‚±‚إپAگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚ج‰ءگ…•ھ‰ً’èگ”‚ًKhپAگ|ژ_CH3COOH‚جژ_‰ً—£’èگ”‚ًKaپAگ…‚جƒCƒIƒ“گد‚ًKw‚ئ‚·‚é‚ئپAژں‚ج‚و‚¤‚ة‚ب‚è‚ـ‚·پB

‚½‚¾‚µپA‚±‚ê‚حCƒ؟ پ†10-6 ‚جڈًŒڈ‚ھگ¬—§‚µ‚ؤ‚¢‚éڈêچ‡‚ةŒہ‚è‚ـ‚·پB‚à‚µCƒ؟پƒ10-6 ‚ب‚ç‚خپAگ…H2O‚جڈo‚·گ…ژ_‰»•¨ƒCƒIƒ“OH- ‚جٹٌ—^‚ً–³ژ‹‚إ‚«‚ب‚‚ب‚ء‚ؤ‚µ‚ـ‚¤‚ج‚إ‚·پBگ…H2O‚ج“d—£‚ـ‚إچl‚¦‚é‚ئپA[OH-]‚ً‹پ‚ك‚éژ®‚ح‘ه•د•،ژG‚ة‚ب‚è‚ـ‚·پB‚±‚ê‚ًژèŒvژZ‚إ‰ً‚‚ج‚حچ¢“ï‚ب‚½‚كپAژمژ_‚ئ‹‰–ٹî‚ج‰–‚ھ‰ءگ…•ھ‰ً‚·‚éڈêچ‡‚إ‚àپACƒ؟ پ†10-6 ‚جڈًŒڈ‚ھ–³ڈًŒڈ‚ةگ¬—§‚µ‚ؤ‚¢‚é‚ئچl‚¦‚ؤ–â‘è‚ ‚è‚ـ‚¹‚ٌپB‚ـ‚½پA‰ءگ…•ھ‰ً“xƒ؟‚ح’تڈيƒ؟ <<1‚ب‚ج‚إپAˆê”ت“I‚ةC mol/L‚جژمژ_پ{‹‰–ٹî‚ج‰–‚ج[OH-]‚حپAژں‚ج‚و‚¤‚ة•\‚·‚±‚ئ‚ھ‚إ‚«‚ـ‚·پB
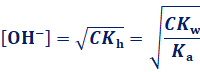
پ¦‚½‚¾‚µپACƒ؟ پ†10-6 ‚ج‚ئ‚«‚ةŒہ‚é
(7) ‹ژ_پ{ژم‰–ٹî‚ج‰–‚ھ‰ءگ…•ھ‰ً‚·‚éڈêچ‡(‹ژ_پ{ژم‰–ٹî‚ج’†کa“_‚جpH)
پ@‹ژ_‚ئژم‰–ٹî‚ج’†کa‚ة‚و‚ء‚ؤگ¶‚¶‚鉖‚ھگ…H2O‚ة—n‚¯‚é‚ئپA‰ءگ…•ھ‰ً‚ھ‹N‚±‚ء‚ؤژمژ_گ«‚ًژ¦‚µ‚ـ‚·پB‚±‚±‚إپAC mol/L‚ج‰–‰»ƒAƒ“ƒ‚ƒjƒEƒ€NH4Clگ…—n‰t‚ج[H+]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پB‰–‰»ƒAƒ“ƒ‚ƒjƒEƒ€NH4Cl‚حپAگ…—n‰t’†‚إ‚ح100%‚ھ“d—£‚µ‚ؤ‚¨‚èپAƒAƒ“ƒ‚ƒjƒEƒ€ƒCƒIƒ“NH4+‚ئ‰–‰»•¨ƒCƒIƒ“Cl- ‚ئ‚ة“d—£‚µ‚ؤ‚¢‚ـ‚·پB‰–‰»•¨ƒCƒIƒ“Cl- ‚حگ…H2O‚ئ‚ح”½‰‚µ‚ـ‚¹‚ٌ‚ھپAƒAƒ“ƒ‚ƒjƒEƒ€ƒCƒIƒ“NH4+‚جˆê•”‚حگ…H2O‚ئ”½‰‚µ‚ـ‚·پB‚±‚±‚إپA‰–‰»ƒAƒ“ƒ‚ƒjƒEƒ€NH4Cl‚ج‰ءگ…•ھ‰ً’èگ”‚ًKhپAƒAƒ“ƒ‚ƒjƒANH3‚ج‰–ٹî—£’èگ”‚ًKbپAگ…‚جƒCƒIƒ“گد‚ًKw‚ئ‚·‚é‚ئپAژں‚ج‚و‚¤‚ة‚ب‚è‚ـ‚·پB

‚½‚¾‚µپA‚±‚ê‚حCƒ؟ پ†10-6 ‚جڈًŒڈ‚ھگ¬—§‚µ‚ؤ‚¢‚éڈêچ‡‚ةŒہ‚è‚ـ‚·پB‚à‚µCƒ؟پƒ10-6 ‚ب‚ç‚خپAگ…H2O‚جڈo‚·گ…‘fƒCƒIƒ“H+ ‚جٹٌ—^‚ً–³ژ‹‚إ‚«‚ب‚‚ب‚ء‚ؤ‚µ‚ـ‚¤‚ج‚إ‚·پBگ…H2O‚ج“d—£‚ـ‚إچl‚¦‚é‚ئپA[H+]‚ً‹پ‚ك‚éژ®‚ح‘ه•د•،ژG‚ة‚ب‚è‚ـ‚·پB‚±‚ê‚ًژèŒvژZ‚إ‰ً‚‚ج‚حچ¢“ï‚ب‚½‚كپA‹ژ_‚ئژم‰–ٹî‚ج‰–‚ھ‰ءگ…•ھ‰ً‚·‚éڈêچ‡‚إ‚àپACƒ؟ پ†10-6 ‚جڈًŒڈ‚ھ–³ڈًŒڈ‚ةگ¬—§‚µ‚ؤ‚¢‚é‚ئچl‚¦‚ؤ–â‘è‚ ‚è‚ـ‚¹‚ٌپB‚ـ‚½پA‰ءگ…•ھ‰ً“xƒ؟‚ح’تڈيƒ؟ <<1‚ب‚ج‚إپAپAˆê”ت“I‚ةC mol/L‚ج‹ژ_پ{ژم‰–ٹî‚ج‰–‚ج[H+]‚حپAژں‚ج‚و‚¤‚ة•\‚·‚±‚ئ‚ھ‚إ‚«‚ـ‚·پB
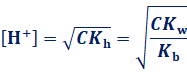
پ¦‚½‚¾‚µپACƒ؟ پ†10-6 ‚ج‚ئ‚«‚ةŒہ‚é
پ@ڈƒگ…H2O‚ة‹ژ_‚⋉–ٹî‚ًڈ—ت‰ء‚¦‚é‚ئپA‚»‚جpH‚ح‘ه‚«‚•د‰»‚µ‚ـ‚·پB‚µ‚©‚µپAگ|ژ_CH3COOH‚ئگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚جچ¬چ‡گ…—n‰t‚ة‹ژ_‚⋉–ٹî‚ًڈ—ت‰ء‚¦‚ؤ‚àپApH‚ج•د‰»‚حڈ¬‚³‚¢‚إ‚·پB‚±‚ج‚و‚¤‚ةپAژ_‚≖ٹî‚ً‰ء‚¦‚½‚ئ‚«‚ةpH•د‰»‚ًڈ¬‚³‚‚·‚éچى—p‚ًپuٹةڈصچى—p(buffer action)پv‚ئ‚¢‚¢پA‚±‚جچى—p‚ج‘ه‚«‚ب—n‰t‚ًپuٹةڈص‰t(buffer solution)پv‚ئ‚¢‚¢‚ـ‚·پB
—ل‚¦‚خپAŒŒ‰t‚حگg‹ك‚بٹةڈص‰t‚إ‚·پBŒŒ‰t‚ة‚حٹةڈصچى—p‚ھ‚ ‚é‚ج‚إپAٹO•”‚©‚瑽ڈ‚جˆظ•¨‚ھ“ü‚èچ‚ٌ‚إ‚àپA’v–½“I‚ب‰e‹؟‚ھگ¶‚¶‚ب‚¢‚و‚¤‚ة‚ب‚ء‚ؤ‚¢‚é‚ج‚إ‚·پBŒŒ‰t‚حپA’Yژ_H2CO3‚ئ’Yژ_گ…‘fƒCƒIƒ“HCO3- ‚ئ‚ج“d—£•½چt‚ة‚و‚èپAٹةڈصچى—p‚ًٹl“¾‚µ‚ؤ‚¨‚èپAژم‰–ٹîگ«(pHپپ7.4)‚ة•غ‚½‚ê‚ؤ‚¢‚ـ‚·پB‚ـ‚½پA‘ء‰t‚ة‚à’Yژ_گ…‘fƒCƒIƒ“HCO3- ‚ھٹـ‚ـ‚ê‚ؤ‚¨‚èپAژ_‚ء‚د‚¢‚à‚ج‚ًگH‚ׂ½‚ئ‚«‚ةپAٹةڈصچى—p‚ة‚و‚ء‚ؤژ_–،‚ًکa‚ç‚°‚é“‚«‚ً‚µ‚ؤ‚¢‚ـ‚·پB”~ٹ±‚µ‚⃌ƒ‚ƒ“‚ب‚ا‚ًگH‚ׂé‚ئ‚«‚ةپA‘ء‰t‚ھ‘ه—ت‚ة•ھ”ه‚³‚ê‚é‚ج‚ح‚±‚ج‚½‚ك‚إ‚·پBˆê”ت“I‚ةژمژ_‚ئ‚»‚ج‰–‚âژم‰–ٹî‚ئ‚»‚ج‰–‚جچ¬چ‡—n‰t‚حپAٹةڈصچى—p‚ًژ‚آ‚ج‚إ‚·پB
H2CO3پ@⇄پ@ HCO3-پ@پ{پ@H+
پ@—ل‚ئ‚µ‚ؤپAگ|ژ_CH3COOH‚ئگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚جچ¬چ‡—n‰t‚جژ‚آٹةڈصچى—p‚ًچl‚¦‚ؤ‚ف‚ـ‚µ‚ه‚¤پBگ|ژ_CH3COOH‚ئگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚حپAگ…—n‰t’†‚إ‚حژں‚ج‚و‚¤‚ة“d—£‚µ‚ؤ‚¢‚ـ‚·پB
CH3COOHپ@⇄پ@CH3COO-پ@پ{پ@H+
CH3COONaپ@پ¨پ@CH3COO-پ@پ{پ@Na+
گ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚حƒCƒIƒ“Œ‹چ‡گ«‚ج‰–‚ب‚ج‚إپA‚»‚ج‚ظ‚ئ‚ٌ‚ا‚ھ“d—£‚µ‚ؤپAگ|ژ_ƒCƒIƒ“CH3COO- ‚ة‚ب‚ء‚ؤ‚¢‚ـ‚·پB‚µ‚©‚µپAگ|ژ_CH3COOH‚حژمژ_‚ب‚ج‚إپA‚»‚ج‚ظ‚ئ‚ٌ‚ا‚ح“d—£‚¹‚¸‚ةگ|ژ_CH3COOH‚ج‚ـ‚ـ‚إ‚·پB‚و‚ء‚ؤپA‚±‚جچ¬چ‡‰t‚ة‚¨‚¢‚ؤ‚حپAژں‚ج‚و‚¤‚بٹضŒW‚ھگ¬‚è—§‚؟‚ـ‚·پB
[CH3COO-]پپ‰ء‚¦‚½CH3COONa
[CH3COOH]پپ‰ء‚¦‚½CH3COOH
‚»‚±‚إپA‚±‚جچ¬چ‡—n‰t‚ةژ_‚≖ٹî‚ًڈ—ت‰ء‚¦‚é‚ئپAژں‚ج‚و‚¤‚ب”½‰‚ھ‹N‚±‚èپA‰ء‚¦‚½گ…‘fƒCƒIƒ“H+ ‚âگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ھ’†کa‚³‚ê‚ـ‚·پB
ژ_‚ً‰ء‚¦‚½‚ئ‚«پFCH3OO-پ@پ{پ@H+پ@پ¨پ@CH3COOH
‰–ٹî‚ً‰ء‚¦‚½‚ئ‚«پFCH3COOHپ@پ{پ@OH-پ@پ¨پ@CH3COO-پ@پ{پ@H2O
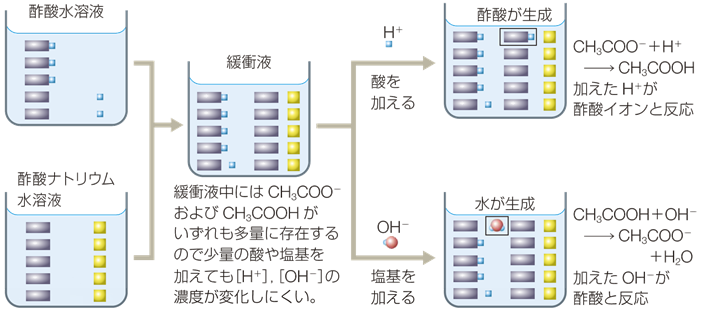
گ}.1 گ|ژ_CH3COOH‚ئگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚جٹةڈص‰t
ژ_‚≖ٹî‚ً‰ء‚¦‚½‚ئ‚«‚ج”½‰‚حپA‚ظ‚ع100%‰E‚ةگi‚ق”½‰‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپAڈ—ت‚جگ…‘fƒCƒIƒ“H+ ‚âگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ً‰ء‚¦‚ؤ‚àپA[H+]‚â[OH-]‚ج•د‰»‚ھ—}‚¦‚ç‚êپApH‚ج•د‰»‚ھٹة‚â‚©‚ة‚ب‚é‚ج‚إ‚·پB‚±‚±‚إپACa mol/L‚جگ|ژ_CH3COOH‚ئCs mol/L‚جگ|ژ_ƒiƒgƒٹƒEƒ€CH3COONa‚جچ¬چ‡—n‰t‚ج[H+]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پB
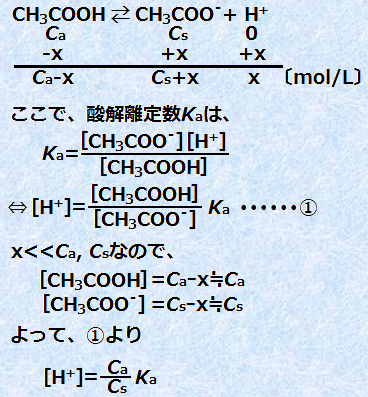
‚±‚جژ®‚و‚èپAٹةڈص‰t‚ج[H+]‚حCa ,Cs, Ka‚ةˆث‘¶‚·‚邱‚ئ‚ھ•ھ‚©‚è‚ـ‚·پB‚ـ‚½پAKa‚ح‰·“xˆê’è‚ب‚çˆê’è’l‚ة‚ب‚é‚ج‚إپAژہژ؟پAٹةڈص‰t‚جpH‚حCa ,Cs‚ة‚و‚茈’肳‚ê‚é‚ئ‚¢‚¤‚±‚ئ‚à•ھ‚©‚è‚ـ‚·پB‚±‚جٹةڈص‰t‚ةژ_‚ً‰ء‚¦‚é‚ئCs‚ھŒ¸‚ء‚ؤCa‚ھ‘‚¦پA‰–ٹî‚ً‰ء‚¦‚é‚ئCa‚ھŒ¸‚ء‚ؤCs‚ھ‘‚¦‚邱‚ئ‚و‚èپAٹةڈص‰t‚ج[H+]‚ح—eˆص‚ة‹پ‚ك‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پB
—ل‚ئ‚µ‚ؤپAƒAƒ“ƒ‚ƒjNH3‚ئ‰–‰»ƒAƒ“ƒ‚ƒjƒEƒ€NH4Cl‚جچ¬چ‡—n‰t‚جژ‚آٹةڈصچى—p‚ًچl‚¦‚ؤ‚ف‚ـ‚µ‚ه‚¤پBƒAƒ“ƒ‚ƒjƒANH3‚ئ‰–‰»ƒAƒ“ƒ‚ƒjƒEƒ€NH4Cl‚حپAگ…—n‰t’†‚إ‚حژں‚ج‚و‚¤‚ة“d—£‚µ‚ؤ‚¢‚ـ‚·پB
NH3پ@پ{پ@H2Oپ@⇄پ@NH4+پ@پ{پ@OH-
NH4Clپ@پ¨پ@NH4+پ@پ{پ@Cl-
‰–‰»ƒAƒ“ƒ‚ƒjƒEƒ€NH4Cl‚حƒCƒIƒ“Œ‹چ‡گ«‚ج‰–‚ب‚ج‚إپA‚»‚ج‚ظ‚ئ‚ٌ‚ا‚ھ“d—£‚µ‚ؤپAƒAƒ“ƒ‚ƒjƒEƒ€ƒCƒIƒ“NH4+ ‚ة‚ب‚ء‚ؤ‚¢‚ـ‚·پB‚µ‚©‚µپAƒAƒ“ƒ‚ƒjƒANH3‚حژم‰–ٹî‚ب‚ج‚إپA‚»‚ج‚ظ‚ئ‚ٌ‚ا‚ح“d—£‚¹‚¸‚ةƒAƒ“ƒ‚ƒjƒANH3‚ج‚ـ‚ـ‚إ‚·پB‚و‚ء‚ؤپA‚±‚جچ¬چ‡‰t‚ة‚¨‚¢‚ؤ‚حپAژں‚ج‚و‚¤‚بٹضŒW‚ھگ¬‚è—§‚؟‚ـ‚·پB
[NH4+]پپ‰ء‚¦‚½NH4Cl
[NH3] پپ‰ء‚¦‚½NH3
‚»‚±‚إپA‚±‚جچ¬چ‡—n‰t‚ةژ_‚≖ٹî‚ًڈ—ت‰ء‚¦‚é‚ئپAژں‚ج‚و‚¤‚ب”½‰‚ھ‹N‚±‚èپA‰ء‚¦‚½گ…‘fƒCƒIƒ“H+ ‚âگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ھ’†کa‚³‚ê‚ـ‚·پB
ژ_‚ً‰ء‚¦‚½‚ئ‚«پFNH3پ@پ{پ@H+پ@پ¨پ@NH4+
‰–ٹî‚ً‰ء‚¦‚½‚ئ‚«پFNH4+پ@پ{پ@OH-پ@پ¨پ@NH3پ@پ{پ@H2O
ژ_‚≖ٹî‚ً‰ء‚¦‚½‚ئ‚«‚ج”½‰‚حپA‚ظ‚ع100%‰E‚ةگi‚ق”½‰‚إ‚·پB‚µ‚½‚ھ‚ء‚ؤپAڈ—ت‚جگ…‘fƒCƒIƒ“H+ ‚âگ…ژ_‰»•¨ƒCƒIƒ“OH- ‚ً‰ء‚¦‚ؤ‚àپA[H+]‚â[OH-]‚ج•د‰»‚ھ—}‚¦‚ç‚êپApH‚ج•د‰»‚ھٹة‚â‚©‚ة‚ب‚é‚ج‚إ‚·پB‚±‚±‚إپACb mol/L‚جƒAƒ“ƒ‚ƒjƒANH3‚ئCs mol/L‚ج‰–‰»ƒAƒ“ƒ‚ƒjƒEƒ€NH4Cl‚جچ¬چ‡—n‰t‚ج[OH-]‚ً‹پ‚ك‚ؤ‚ف‚ـ‚µ‚ه‚¤پB
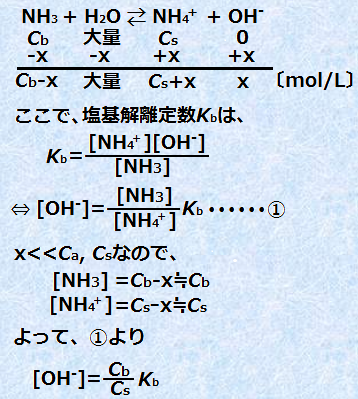
‚±‚جژ®‚و‚èپAٹةڈص‰t‚ج[OH-]‚حCb ,Cs, Kb‚ةˆث‘¶‚·‚邱‚ئ‚ھ•ھ‚©‚è‚ـ‚·پB‚ـ‚½پAKb‚ح‰·“xˆê’è‚ب‚çˆê’è’l‚ة‚ب‚é‚ج‚إپAژہژ؟پAٹةڈص‰t‚جpH‚حCb ,Cs‚ة‚و‚茈’肳‚ê‚é‚ئ‚¢‚¤‚±‚ئ‚à•ھ‚©‚è‚ـ‚·پB‚±‚جٹةڈص‰t‚ةژ_‚ً‰ء‚¦‚é‚ئCb‚ھŒ¸‚ء‚ؤCs‚ھ‘‚¦پA‰–ٹî‚ً‰ء‚¦‚é‚ئCs‚ھŒ¸‚ء‚ؤCb‚ھ‘‚¦‚邱‚ئ‚و‚èپAٹةڈص‰t‚ج[OH-]‚ح—eˆص‚ة‹پ‚ك‚邱‚ئ‚ھ‚إ‚«‚ـ‚·پB
پEژQچl•¶Œ£
1) گخگىگ³–¾پuگV—Œn‚ج‰»ٹw(ڈم)پvڈx‘ن•¶Œة(2005”N”چs)